Podaj wzór powstałej soli.
NH4H2PO4

![]()
Ze 132 g siarczanu (VI) amonu powstaje 34 g amoniaku.
Ilość powstała z 52,8 g soli:
132 g – 34 g
52,8 g – x
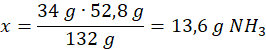
Ilość moli amoniaku:
17 g – 1 mol
13,6 g – y
![]()
Ilość kwasu fosforowego, z którym zareagował amoniak:
98 g – 1 mol
78,4 g – z moli
![]()
Widzimy, że substraty były zmieszane w stosunku molowym 1 : 1 – tak też zapisujemy reakcje i szukamy takiego produkty, żeby reakcja była zbilansowana.
![]()
Tym produktem jest diwodorofosforan (V) amonu.

Ćwiczenie 12.3.
246Ćwiczenie 12.6.
246Ćwiczenie 12.9.
246Ćwiczenie 12.10.
246Ćwiczenie 12.11.
246Ćwiczenie 12.32.
248Ćwiczenie 12.33.
248Ćwiczenie 12.39.
249Ćwiczenie 12.46.
249Ćwiczenie 12.50.
250Ćwiczenie 12.52.
250Ćwiczenie 12.54.
250Ćwiczenie 12.56.
250Ćwiczenie 12.58.
250Ćwiczenie 12.59.
251Ćwiczenie 12.60.
251Ćwiczenie 12.62.
251Ćwiczenie 12.64.
251Ćwiczenie 12.65.
251Ćwiczenie 12.66.
251Ćwiczenie 12.70.
252Ćwiczenie 12.98.
255Ćwiczenie 12.99.
255Ćwiczenie 12.100.
255Ćwiczenie 12.101.
255Ćwiczenie 12.102.
255Ćwiczenie 12.103.
255Ćwiczenie 12.104.
255Ćwiczenie 12.109.
256Ćwiczenie 12.110.
256Ćwiczenie 12.120.
257
