Beryl, min 72%, max. 90%

Krok 1. Ilość moli wodoru. W warunkach normalnych 1 mol ma objętość 22,4 dm3
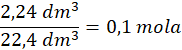
Krok 2. Ilość moli metalu – wykorzystaj dane z poprzedniego zadania.
Aby otrzymać 0,1 mola wodoru potrzeba 0,2 mola metalu jednowartościowego, 0,1 mola metalu dwuwartościowego i 0,067 mola metalu trójwartościowego. Próbka ma 1 g. Obliczamy masy molowe pierwiastków, które w 1 g zawierają podane wartości moli:
0,2 mola – 1 g
1 mol – x g
![]()
0,1 mola – 1 g
1 mol – y
![]()
0,067 mola – 1 g
1 mol – z
![]()
Z obliczonych mas jedynie masa 10 g jest zbliżona do masy metalu z układu okresowego – berylu (9 g/mol)
Krok 2. Maksymalna zawartość metalu.
Aby uzyskać 0,1 mola wodoru potrzebne jest 0,1 mola berylu.
1 mol – 9 g
0,1 mola – x
![]()
Próbka ma 1 g:
![]()
Krok 3. Minimalna zawartość metalu.
W poprzednim zadaniu ustalono, że drugim metalem, co do ilości wydzielonego wodoru jest lit, przyjmij więc, że mamy mieszaninę litu i berylu o masie 1 g. Na 1 mol litu wydziela się 0,5 mola wodoru.
x – ilość berylu, y – ilość litu
![]()
![]()
![]()
![]()
![]()
![]()
![]()
Masa berylu:
![]()
Zawartość w próbce:
![]()