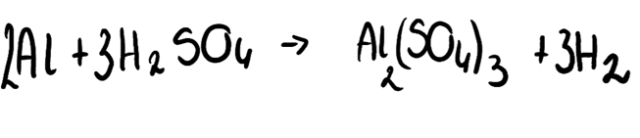Wybierz w każdym zdaniu właściwe uzupełnienie tak, aby zdania były prawdziwe.
Z kwasem jodowodorowym nie będzie reagował pierwiastek o konfiguracji elektronów walencyjnych 5s14d10. Po umieszczeniu w rozcieńczonym roztworze kwasu siarkowego(VI) oczyszczonej mechanicznie blaszki glinu zaobserwujemy wydzielanie się bezbarwnego, bezwonnego gazu. Silniejsze właściwości utleniające w porównaniu z Sn2+ wykazują jony ołowiu. Słabsze właściwości redukujące w porównaniu z właściwościami metalicznego kobaltu wykazują metale o wyższej niż -0,28 V wartości potencjału standardowego. Dlatego jony Co2+ nie mogą zostać zredukowane przez metaliczna miedź.

1. Z kwasem jodowodorowym nie będzie reagował pierwiastek o konfiguracji elektronów walencyjnych 5s14d10 (miedź) // Silniejsze właściwości utleniające w porównaniu z Sn2+ wykazują jony ołowiu. Słabsze właściwości redukujące w porównaniu z właściwościami metalicznego kobaltu wykazują metale o wyższej niż -0,28 V wartości potencjału standardowego. Dlatego jony Co2+ nie mogą zostać zredukowane przez metaliczna miedź:
· Aby porównać aktywność pierwiastków, należy skorzystać z szeregu elektrochemicznego metali.
· Im niższy potencjał standardowy, tym większa aktywność pierwiastka. Mniej aktywny pierwiastek nie wyprze bardziej aktywnego z roztworu jego kwasu czy soli.
· Im niższy potencjał standardowy, tym większa zdolność pierwiastka do utleniania się- większe jego właściwości redukujące.
· Niektóre pierwiastki w kontakcie z kwasami utleniającymi ulegają pasywacji- pokrywają się ochronną warstwą tlenków, w związku z czym nie mogą z tymi kwasami reagować.
2. Po umieszczeniu w rozcieńczonym roztworze kwasu siarkowego(VI) oczyszczonej mechanicznie blaszki glinu zaobserwujemy wydzielanie się bezbarwnego, bezwonnego gazu: