Ustal wzór sumaryczny tego związku chemicznego.

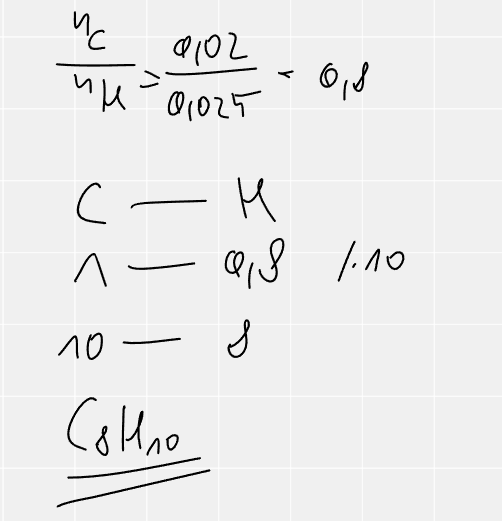
W pierwszej części zadania sprawdzono, czy badany związek był węglowodorem, czy zawierał inne pierwiastki/podstawniki. Wykazano, że związek jest węglowodorem z wykorzystaniem prawa zachowania masy. Wykorzystując obliczone ilości moli węgla i wodoru w związku obliczono stosunek molowy C do H. Znając ten stosunek oraz masę molową związku odpowiedzią jest C8H10.

Aby ustalić wzór sumaryczny związku chemicznego na podstawie danych ze spalania, najpierw obliczamy liczbę moli dwutlenku węgla (CO₂) i pary wodnej (H₂O), które powstały podczas reakcji. Wiemy, że każdy mol CO₂ pochodzi od jednego mola atomów węgla (C), a każdy mol H₂O zawiera dwa atomy wodoru (H), więc na podstawie ilości powstałych produktów możemy wyznaczyć ilość atomów węgla i wodoru w badanym związku.
Następnie, korzystając z mas molowych węgla i wodoru, obliczamy ich łączną masę w próbce. Odejmując tę masę od całkowitej masy próbki związku, otrzymujemy masę tlenu (O). Znając masę tlenu, przeliczamy ją na liczbę moli tlenu, korzystając z masy molowej tlenu. Po obliczeniu liczby moli węgla, wodoru i tlenu ustalamy ich stosunek molowy, dzieląc wszystkie wartości przez najmniejszą spośród nich, co pozwala otrzymać najprostszy stosunek całkowity – czyli wzór empiryczny związku.
Na koniec, znając masę molową związku, porównujemy ją z masą molową wzoru empirycznego, aby określić, ile razy wzór empiryczny powtarza się w rzeczywistym wzorze sumarycznym. Mnożąc odpowiednio wszystkie indeksy we wzorze empirycznym, uzyskujemy ostateczny wzór sumaryczny badanego związku chemicznego.

Zadanie 11
18Zadanie 12
19Zadanie 8
25Zadanie 18
29Zadanie 22
30Zadanie 30
33Zadanie 32
34Zadanie 36
35Zadanie 45
38Zadanie 53
41Zadanie 3
49Zadanie 5
50Zadanie 8
51Zadanie 10
52Zadanie 11
52Zadanie 15
54Zadanie 18
56Zadanie 22
57Zadanie 32
61Zadanie 34
62Zadanie 42
65Zadanie 47
70Zadanie 48
71Zadanie 50
72Zadanie 52
73Zadanie 53
73Zadanie 55
74Zadanie 60
76Zadanie 68
79Zadanie 79
83Zadanie 89
88Zadanie 92
89Zadanie 95
90Zadanie 101
93Zadanie 103
94Zadanie 11*
101Zadanie 15
103Zadanie 19
104Zadanie 26
107Zadanie 28
108Zadanie 30
109Zadanie 33
110Zadanie 39
113Zadanie 53
117Zadanie 55
118Zadanie 56
118Zadanie 58
119Zadanie 63
122Zadanie 67
123
