a) lit, Li
b)
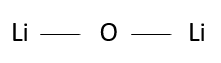

c) 2 Li+, O2-

Cyfra jedności w numerze grupy określa liczbę elektronów walencyjnych. Numer okresu określa liczbę powłok elektronowych. Pierwiastek o konfiguracji elektronowej [2, 1] znajduje się w 1. grupie i 2. okresie. Z układu okresowego pierwiastków chemicznych można odczytać, że jest to lit. Tlen posiada 6 elektronów walencyjnych. Do osiągnięcia oktetu elektronowego brakuje mu 2 elektronów. Lit posiada 1 elektron walencyjny. W celu uzyskania oktetu elektronowego atom tlenu musi utworzyć wiązania z 2 atomami litu. W wyniku łączenia się atomów litu z atomami tlenu, atomy litu oddają elektrony walencyjne i stają się jonami dodatnimi (kationami), natomiast atom tlenu przyjmuje elektrony walencyjne i staje się jonem ujemnym (anionem). 2 atomy litu oddały po jednym elektronie walencyjnym, więc ich zapis to: 2 Li+. Atom tlenu przyjął 2 elektrony walencyjne, więc jego zapis to: O2-.