| NaCl | NCl3 | CO2 |
| Spodziewane wiązanie chemiczne:∆E=3,0-0,9=2,1 jonowe | Spodziewane wiązanie chemiczne:∆E=3,0-3,0=0 kowalencyjne niespolaryzowane | Spodziewane wiązanie chemiczne:∆E=3,5-2,5=1 kowalencyjne spolaryzowane |
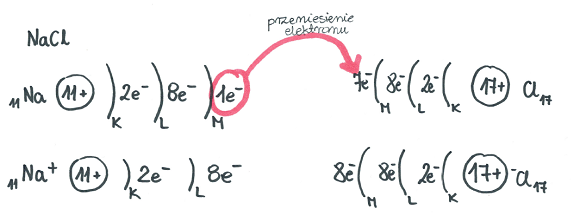
| Szkic wiązania jonowego opisany został na dołączonej poniżej grafice. | Szkic wiązań:Cl – N – Cl|Cl | Szkic wiązań:O = C = O |

Elektroujemność – miara siły przyciągania elektronów w atomie, tworzących wiązania w cząsteczce przez atomy danego pierwiastka chemicznego.
Rodzaje wiązań w zależności od zakresu elektroujemności:
Wiązanie kowalencyjne niespolaryzowane – 0≤∆E≤0,4
Wiązanie kowalencyjne spolaryzowane – 0,4<∆E<1,7
Wiązanie jonowe – ∆E≥1,7
Wartości te pozwalają określić, jakie wiązanie występuje między pierwiastkami.