Mamy wybrać pierwiastek spośród: azot, wanad, mangan, arsen, który:
· ma 5 elektronów walencyjnych,
· ma 11 elektronów na powłoce M.
Zatem:
· azot (N, Z=7) → powłoka M pusta, odpada
· wanad (V, Z=23) → konfiguracja:
![]()
na powłoce M:
![]() , elektrony walencyjne:
, elektrony walencyjne:
![]() → razem 5
→ razem 5
· mangan (Mn, Z=25) → na powłoce M byłoby 13
· arsen (As, Z=33) → na powłoce M byłoby 18
Szukanym pierwiastkiem jest wanad (V).
Pełna powłokowa konfiguracja elektronowa: K2 L8 M11 N2
Skrócona podpowłokowa konfiguracja elektronowa: [Ar] 3d3 4s2
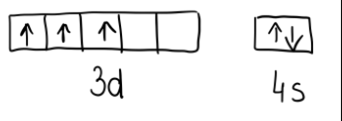
Konfiguracja elektronów walencyjnych w systemie klatkowym: