W tym zadaniu musisz określić, z której z podanych reakcji otrzyma się więcej pary wodnej.
1) 2H2 + O2→ 2H2O
4u H2 odpowiadają 36u H2O
1 g H2 odpowiada x g H2O
![]()
4x = 36
x = 9 g H2O
2) Cu2O + H2 → 2Cu + H2O
2u H2 odpowiadają 18u H2O
1 g H2 odpowiada y g H2O
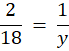
2y = 18
y = 9 g H2O
Odpowiedź: W obu przypadkach powstaje tyle samo pary wodnej: 9 g.

Rozpisz równanie reakcji chemicznej. Pamiętaj, aby dobrać odpowiednie współczynniki stechiometryczne. Za pomocą proporcji zestaw ze sobą informacje o masach z treści zadania (niewiadomą masy pary wodnej z 1 g H2) oraz informacje o ich masach atomowych/cząsteczkowych na podstawie układu okresowego pierwiastków, które biorą udział w tej reakcji. Postąp tak z obiema reakcjami. Oblicz niewiadome. Porównaj wyniki.

Zadanie 2.1.1.
23Zadanie 2.1.2.
23Zadanie 2.1.3.
23Zadanie 2.1.4.
23Zadanie 2.1.5.
23Zadanie 2.1.7.
23Zadanie 2.1.8.
24Zadanie 2.1.9.
24Zadanie 2.1.12.
25Zadanie 2.1.13.
25Zadanie 2.1.14.
25Zadanie 2.1.17.
25Zadanie 2.1.18.
25Zadanie 2.1.19.
25Zadanie 2.1.21.
25Zadanie 2.1.22.
26Zadanie 2.1.23.
26Zadanie 2.2.1.
26Zadanie 2.2.2.
26Zadanie 2.2.3.
26Zadanie 2.2.4.
27Zadanie 2.2.5.
27Zadanie 2.2.6.
27Zadanie 2.2.7.
27Zadanie 2.2.8.
27Zadanie 2.2.16.
28Zadanie 2.2.17.
28Zadanie 2.2.18.
28Zadanie 2.2.19.
28Zadanie 2.2.20.
28Zadanie 2.2.21.
28Zadanie 2.2.22.
28Zadanie 2.2.23.
29Zadanie 2.2.31.
32Zadanie 2.2.32.
32Zadanie 2.2.38.
32Zadanie 2.2.40.
32Zadanie 2.3.1.
32Zadanie 2.3.2.
32Zadanie 2.3.3.
33Zadanie 2.3.4.
33Zadanie 2.3.5.
33Zadanie 2.3.6.
33Zadanie 2.3.7.
33Zadanie 2.3.8.
33Zadanie 2.3.9.
33Zadanie 2.3.10.
33Zadanie 2.3.11.
33Zadanie 2.3.14.
34Zadanie 2.3.20.
35Zadanie 2.3.23.
38Zadanie 2.3.25.
38Zadanie 2.3.29.
38Zadanie 2.3.33.
38
