Oblicz ilość CO2.
pm ≤ 36,4% to:
![]()
pm ≥ 36,4% to:
![]()

Zachodzi reakcja:
![]()
Należy rozważyć dwa przypadki – mieszanina z nadmiarem CO i z nadmiarem tlenu. Zgodnie z równaniem stosunek stechiometryczny to 2 : 1, masa takiej mieszaniny stechiometrycznej to 88 g.
Zawartość tlenu:
![]()
1) pm ≤ 36,4% - nadmiar CO, o ilości produktu decyduje ilość tlenu:
Ilość moli tlenu:
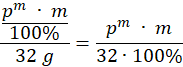
Z równania wynika, że ilość produktu jest dwa razy większa od ilości tlenu:
![]()
2) pm ≥ 36,4% - nadmiar O2, o ilości produktu decyduje ilość CO:
Ilość moli CO:
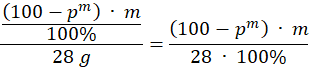
Z reakcji wynika, że ilość moli CO2 jest równa ilości moli CO.

Ćwiczenie 14.1.
261Ćwiczenie 14.3.
261Ćwiczenie 14.4.
261Ćwiczenie 14.6.
261Ćwiczenie 14.7.
261Ćwiczenie 14.9.
261Ćwiczenie 14.10.
261Ćwiczenie 14.14.
262Ćwiczenie **14.25.
262Ćwiczenie 14.26.
264Ćwiczenie 14.28.
264Ćwiczenie 14.30.
264Ćwiczenie 14.31.
264Ćwiczenie 14.32.
264Ćwiczenie 14.33.
264Ćwiczenie 14.34.
264Ćwiczenie 14.35.
264Ćwiczenie 14.37.
265Ćwiczenie 14.39.
265Ćwiczenie *14.44.
265Ćwiczenie *14.51.
266Ćwiczenie 14.52.
266Ćwiczenie 14.53.
266Ćwiczenie 14.54.
266Ćwiczenie 14.57.
266Ćwiczenie 14.58.
266Ćwiczenie 14.80.
268Ćwiczenie 14.85.
268Ćwiczenie 14.86.
269Ćwiczenie 14.87.
269Ćwiczenie 14.88.
269Ćwiczenie 14.91.
269Ćwiczenie 14.93.
269Ćwiczenie 14.94.
269Ćwiczenie *14.107.
270Ćwiczenie 14.115.
271Ćwiczenie 14.116.
271Ćwiczenie 14.120.
271Ćwiczenie 14.121.
271Ćwiczenie 14.122.
271
