Oblicz ilość otrzymanego HNO3.
2 mole

Zachodzi proces:
![]()
![]()
![]()
![]()
![]()
Wykorzystane NO z ostatniego etapu:
![]()
![]()
![]()
Kolejny etap:
![]()
![]()
Kolejne ilości otrzymanego HNO3 to szereg geometryczny (8 moli, 8/3 moli, 8/9 moli):
![]() gdzie α = 8, a q = 1/3
gdzie α = 8, a q = 1/3
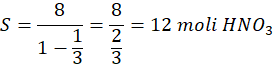
Zakładamy, że wydajność reakcji wynosi 100% (przy użyciu tlenu, wodoru i wody w nadmiarze reaguje cały azot). Z 6 moli N2 powstaje 12 moli HNO3, czyli z 1 mola N2 powstają 2 mole kwasu.

Ćwiczenie 14.1.
261Ćwiczenie 14.3.
261Ćwiczenie 14.4.
261Ćwiczenie 14.6.
261Ćwiczenie 14.7.
261Ćwiczenie 14.9.
261Ćwiczenie 14.10.
261Ćwiczenie 14.14.
262Ćwiczenie **14.25.
262Ćwiczenie 14.26.
264Ćwiczenie 14.28.
264Ćwiczenie 14.30.
264Ćwiczenie 14.31.
264Ćwiczenie 14.32.
264Ćwiczenie 14.33.
264Ćwiczenie 14.34.
264Ćwiczenie 14.35.
264Ćwiczenie 14.37.
265Ćwiczenie 14.39.
265Ćwiczenie *14.44.
265Ćwiczenie *14.51.
266Ćwiczenie 14.52.
266Ćwiczenie 14.53.
266Ćwiczenie 14.54.
266Ćwiczenie 14.57.
266Ćwiczenie 14.58.
266Ćwiczenie 14.80.
268Ćwiczenie 14.85.
268Ćwiczenie 14.86.
269Ćwiczenie 14.87.
269Ćwiczenie 14.88.
269Ćwiczenie 14.91.
269Ćwiczenie 14.93.
269Ćwiczenie 14.94.
269Ćwiczenie *14.107.
270Ćwiczenie 14.115.
271Ćwiczenie 14.116.
271Ćwiczenie 14.120.
271Ćwiczenie 14.121.
271Ćwiczenie 14.122.
271
