SCl2 – dichlorek siarki
ESCl2 = 3,0 - 2,5 = 0,5 wiązanie kowalencyjne spolaryzowane
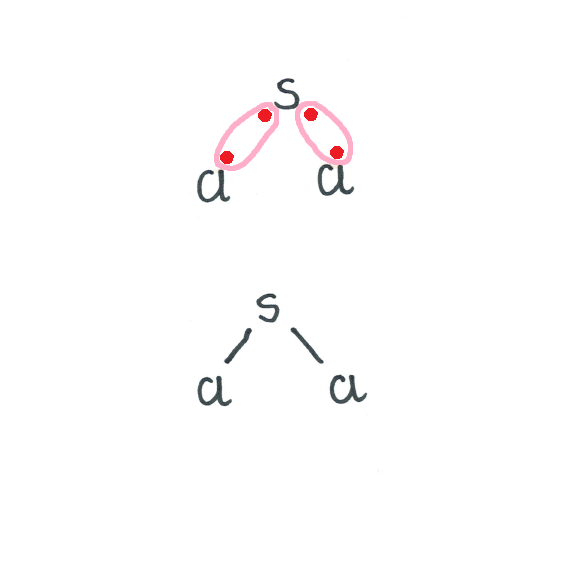
SiCl4 – Tetrachlorek krzemu
ESiCl4 = 3,0-1,8 = 1,2 wiązanie kowalencyjne spolaryzowane
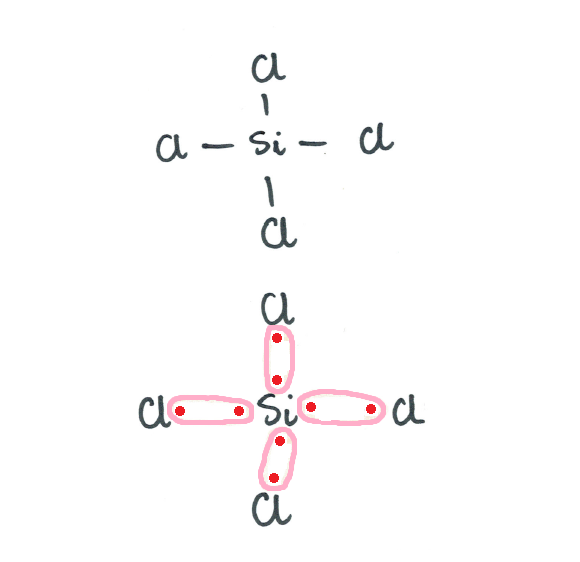
PCl3 – Trichlorek fosforu
EPCl3 = 3,0 - 2,1 = 0,9 wiązanie kowalencyjne spolaryzowane
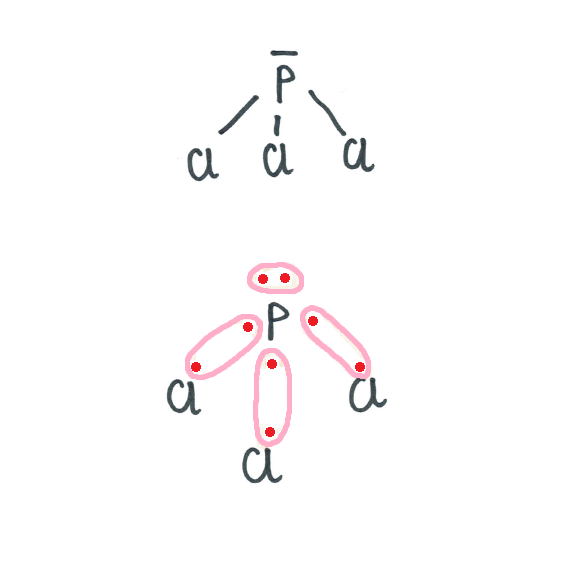
W kolejności wzrastającej polaryzacji: SCl2, PCl3, SiCl4

Skala Paulinga to opracowana w 1932 r. przez Linusa Carla Paulinga skala elektroujemności. Wartości elektroujemności danego pierwiastka możemy odczytać z tablic chemicznych. Elektroujemność jest miarą zdolności przyciągania elektronów przez atom danego pierwiastka chemicznego w trakcie tworzenia wiązania chemicznego.
Rodzaje wiązań w zależności od zakresu elektroujemności:
Wiązanie kowalencyjne niespolaryzowane: – 0 ≤ ∆E ≤ 0,4
Wiązanie kowalencyjne spolaryzowane: – 0,4 < ∆E < 1,7
Wiązanie jonowe: – ∆E ≥ 1,7
Wartości te pozwalają określić, jakie wiązanie występuje między pierwiastkami.