![]() -2266,8 kJ × mol-1
-2266,8 kJ × mol-1

Odpowiednio zapisane zależności termochemiczne pozwalają wyznaczyć entalpie dla określonych reakcji. W podanym zadaniu należało skorzystać z faktu, że entalpia jest wielkością opisującą funkcję stanu.
C3H4(g) + 4 O2(g) ® 3 CO2(g) + 2 H2O(c)
Reakcja spalania propanu:
C3H8(g) + 5 O2(g) ® 3 CO2(g) + 4 H2O(c)
![]()
Reakcja spalania wodoru:
H2(g) + 2 O2(g)® 2 H2O(c). – jest to podwojona reakcja tworzenia wody, więc entalpia tworzenia wody:
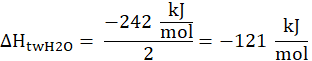
![]()
![]()
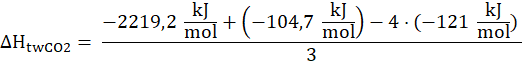
![]()
![]()
![]()
![]() -2266,8 kJ × mol-1
-2266,8 kJ × mol-1