gęstości dwutlenku węgla i wodoru:
d CO2 = 1,977 g/dm3
d H2 = 0,089 g/dm3
równanie reakcji spalania CO:
2CO + O2à 2CO2
wniosek z równania: aby spalić 44,8 dm3 CO potrzebne jest 22,4 dm3 O2
zamień dm3 na m3
44,8 dm3 = 0,0448 m3
22,4 dm3 = 0,0224 m3
za pomocą proporcji oblicz, ilu m3 tlenu odpowiada 500 m3 czadu:
0,0448 m3 CO odpowiada 0,0224 m3 O2
500 m3 CO odpowiada x m3 O2
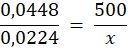
0,0448x = 11,2 / : 0,0448
x = 250 m3 O2
równanie reakcji spalania H2:
2H2 + O2à 2H2O
wniosek z równania: aby spalić 44,8 dm3 H2 potrzebne jest 22,4 dm3 O2
0,0448 m3 H2 odpowiada 0,0224 m3 O2
500 m3 H2 odpowiada y m3 O2
y = 250 m3 O2
oblicz sumę objętości tlenu potrzebnych do zajścia obu reakcji:
V O2 = 250 m3 O2 + 250 m3 O2 = 500 m3 O2
za pomocą proporcji oblicz objętość powietrza, której 21% stanowi 500 m3:
500 m3 stanowi 21% powietrza
x m3 stanowi 100% powietrza
![]()
50000 = 21x / : 21
x = 2381 m3
Odpowiedź: Objętość zużytego powietrza wynosi 2381 m3.

Pamiętaj, że stała objętości gazu wynosi 22,4 dm3.