W tym zadaniu musisz obliczyć, ile gramów tlenku srebra przereagowało.
równanie reakcji opisanej w zadaniu:
2Ag2O à 4Ag + O2
masy substancji – z treści zadania:
mtlenek srebra = 2 g
msrebro = 1,08 g
jednostkę objętości tlenu zamień na dm3:
Vtlen = 56 cm³ = 0,056 dm3
za pomocą proporcji zestaw ze sobą masę cząsteczkową (Ag2O) i atomową (Ag) oraz masy tych substancji z treści zadania:
2 ∙ 232u Ag2O odpowiada 4 ∙ 108u Ag (z układu okresowego)
x g Ag2O odpowiada 1,08 g Ag (z treści zadania)
oblicz masę tlenku srebra, jaka odpowiada 1,08 g srebra:
x = 1,16 g Ag2O
za pomocą proporcji oblicz masę 0,056 dm3 tlenu:
22,4 dm3 odpowiada 32 g O2
0,056 dm3 odpowiada y g O2
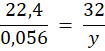
22,4y = 1,792 / : 22,4
y = 0,08 g O2
dodaj do siebie masę srebra z treści zadania i obliczoną masę tlenu:
1,08 g + 0,08 g = 1,16 g Ag2O
za pomocą proporcji oblicz, jaką część 2 g tlenku srebra stanowi 1,16 g tego związku:
2 g Ag2O stanowi 100%
1,16 g Ag2O stanowi z%
![]()
2z = 116
z = 58%
Odpowiedź: Rozkładowi uległo 58% tlenku srebra.

Pamiętaj, że stała objętości gazu wynosi 22,4 dm3.

Zadanie 1.1.6.
7Zadanie 1.1.7.
7Zadanie 1.1.8.
7Zadanie 1.1.13.
8Zadanie 1.1.14.
8Zadanie 1.1.15.
8Zadanie 1.1.16.
8Zadanie 1.1.17.
8Zadanie 1.1.25.
9Zadanie 1.1.27.
10Zadanie 1.1.28.
10Zadanie 1.2.3.
11Zadanie 1.2.4.
11Zadanie 1.2.8.
12Zadanie 1.3.1.
13Zadanie 1.3.2.
13Zadanie 1.3.4.
13Zadanie 1.3.5.
14Zadanie 1.3.7.
14Zadanie 1.3.8.
14Zadanie 1.3.9.
14Zadanie 1.3.11.
15Zadanie 1.3.12.
15Zadanie 1.3.14.
15Zadanie 1.3.24.
17Zadanie 1.3.26.
17Zadanie 1.4.3.
18Zadanie 1.4.6.
18Zadanie 1.4.7.
18Zadanie 1.4.11.
19Zadanie 1.4.12.
19Zadanie 1.4.20.
20Zadanie 1.4.21.
21Zadanie 1.4.24.[WK2]
21
