kwas alkenowy + Br2 → kwas bromoalkanowy
mBr2 = 160 g/mol
1,859 — 160 g
1 — x
x = 1 ∙ 160 : 1,859 = 86,07 ≈ 86 [g]
mCOOH = 45 g/mol
86 g – 45 g = 41 g
wzór ogólny kwasu alkenowego: CnH2n-1COOH
12n + 1 ∙ (2n – 1) = 41
12n + 2n – 1 = 41 / + 1
14 n = 42 / : 14
n = 3 → C3H5COOH → wzór sumaryczny: C4H6O2

Krok 1: Zapisz schemat reakcji. Brom ulega addycji do wiązania podwójnego.
kwas alkenowy + Br2 → kwas bromoalkanowy
Krok 2: Oblicz masę jednej cząsteczki bromu. Pamiętaj, że jest to cząsteczka dwuatomowa.
mBr2 = 2 ∙ 80 = 160 [g/mol]
Krok 3: Zwróć uwagę na proporcje z treści z zadania. Substraty są w stosunku masowym 1 : 1,859. Oznacza to, że cząsteczka bromu to część „1,895”. Na tej podstawie układamy proporcję, by poznać masę kwasu alkenowego.
1,859 — 160 g
1 — x
x = 1 ∙ 160 : 1,859 = 86,07 ≈ 86 [g]
Krok 4: Od masy związku odejmij masę grupy -COOH, by poznać masę pozostałych atomów.
mCOOH = 12 + 16 + 16 + 1 = 45 [g/mol]
86 g – 45 g = 41 g
Krok 5: Zapisz wzór ogólny kwasu alkenowego o jednej grupie -COOH.
CnH2n-1COOH
Krok 6: Znając masę jednego atomy węgla (12 g/mol) i wodoru (1 g/mol) układamy równanie z jedną niewiadomą w postaci liczby atomów węgla n:
12n + 1 ∙ (2n – 1) = 41
12n + 2n – 1 = 41 / + 1
14 n = 42 / : 14
n = 3 → C3H5COOH
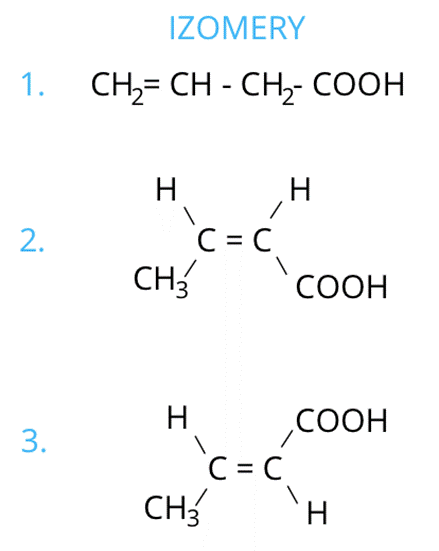
Krok 7: Izomeria. Izomery to związki o tym samym wzorze sumarycznym, ale różnym wzorze strukturalnym. Pierwszym izomerem, niewykazującym diastereoizomerii, jest kwas prop-3-enowy: CH2=CH—CH2—COOH.
Stereoizomeria ma miejsce dla związków nienasyconych, w cząsteczkach których do każdego z atomów węgla przy wiązaniu C=C są przyłączone różne podstawniki. Przy trzecim atomie węgla w kwasie prop-3-enowym są dwa atomy wodoru, więc związek nie tworzy diastereoizomerów.
Kolejnym związkiem o tym samym wzorze sumarycznym jest kwas prop-2-enowy: CH3—CH=CH—COOH. Atom bliższy grupie -COOH ma dwa różne podstawniki: wodór i grupę karboksylową. Drugi atom węgla przy wiązaniu C=C również ma dwa różne podstawniki: wodór i grupę metylową, więc tworzy stereoizomery. Izomeria cis-trans to rodzaj izomerii, który wynika z różnego układu podstawników przy wiązaniu wielokrotnym. Izomeria cis (Z) nakazuje umieszczenie atomów wodoru „po jednej stronie” – nad lub pod linią wiązania wielokrotnego w przypadku przestawiania wzoru w formie półstrukturalnej. Izomeria trans (E) to ułożenie atomów wodoru „po przeciwnych stronach”.