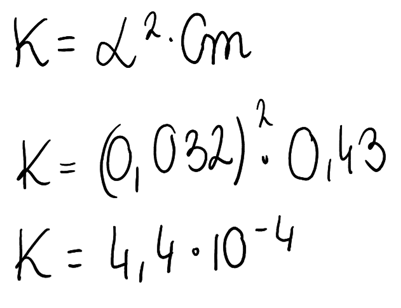1. Znając stężenie procentowe, gęstość i masę molową HNO2, korzystając z odpowiedniego wzoru, możemy obliczyć stężenie molowe całego kwasu:
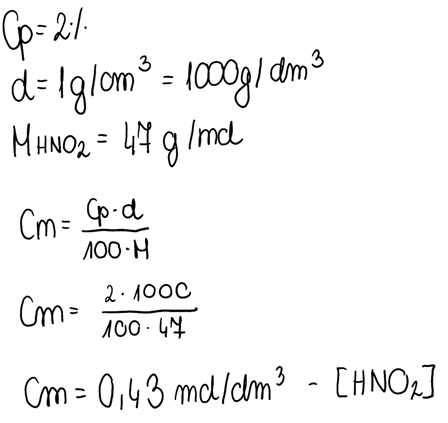
2. Korzystając z przekształconego wzoru na stężenie molowe, obliczamy liczbę moli kwasu w roztworze:
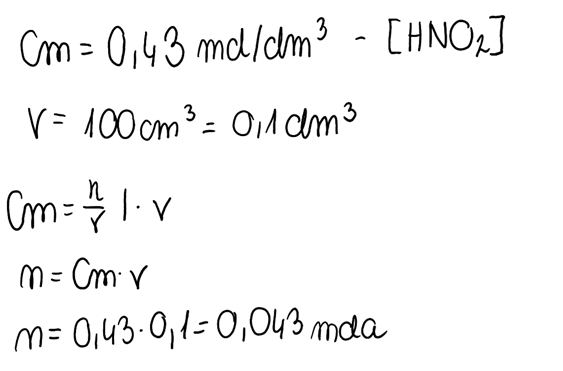
3. Liczbę moli kwasu przeliczamy na cząsteczki, pamiętając, że 1 mol cząsteczek stanowi 6,02*1023 cząsteczek (liczba Avogadro):
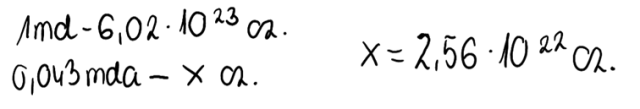
4. Pamiętając, że liczba moli kwasu to suma jego zdysocjowanych i niezdysocjowanych cząsteczek (pamiętaj- HNO2 jest kwasem słabym, który nie dysocjuje całkowicie!), obliczamy liczbę cząsteczek zdysocjowanych. Będzie ona niezbędna do obliczenia stopnia dysocjacji kwasu.
UWAGA: ilość cząsteczek niezdysocjowanych zaczerpnięta jest z treści zadania.
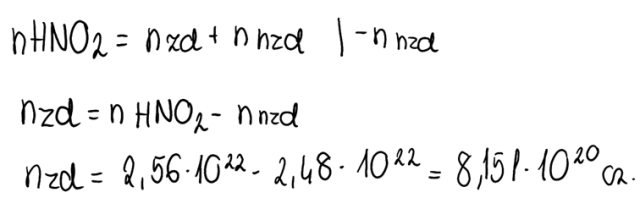
5. Korzystając z wzoru na stopień dysocjacji, obliczamy jego wartość (wyrażoną w %):
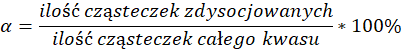
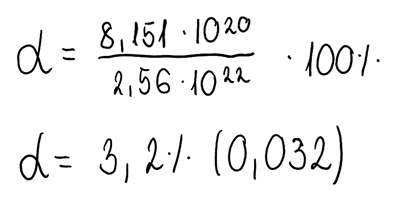
6. Wartość stopnia dysocjacji jest mniejsza niż 5%, zatem zgodnie z prawem rozcieńczeń Ostwalda, możemy skorzystać ze wzoru uproszczonego, aby obliczyć stałej stopnia dysocjacji kwasu: