a) Jest to reakcja egzotermiczna, ponieważ podczas reakcji wydziela się ciepło (∆H = - 156 kJ/mol)
b) Znak zmiany entalpii w tej reakcji chemicznej: ∆H = - 156 kJ/mol, czyli ∆H < 0.
c) Narysuj w zeszycie profil energetyczny tej reakcji chemicznej.
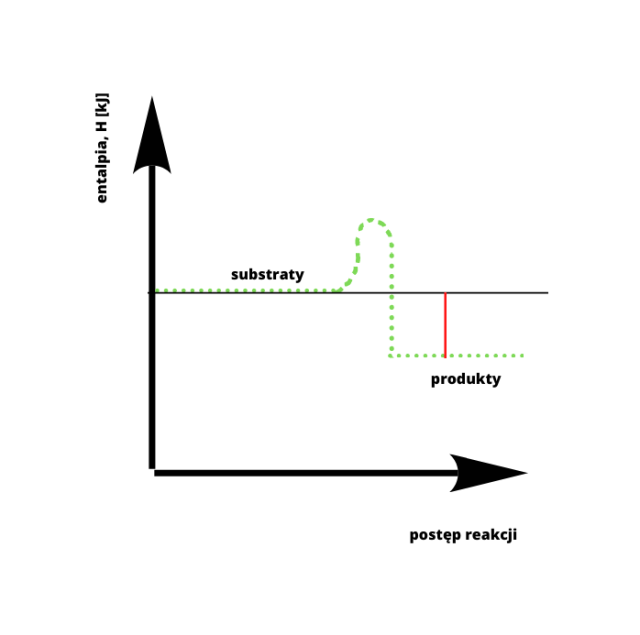
∆H < 0 – zaznaczona na wykresie na czerwono.

X → A ∆H < 0, jest to reakcja egzotermiczna, podczas której zostaje wydzielona energia.
A → Y ∆H > 0, jest to reakcja endotermiczna, do przebiegu której zostaje dostarczona energia.
