Równanie reakcji zobojętniania:
HCl + KOH → A + E
A – KCl
E – H2O
HCl + KOH → KCl + H2O
(lub: A – H2O; E – KCl)
Schemat modelowy tej reakcji:
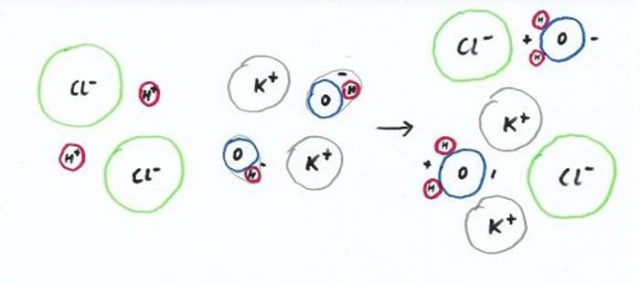

Przedstawione równanie reakcji jest równaniem reakcji zobojętniania. W reakcji zobojętniania kwas reaguje z zasadą, dając jako produkty sól oraz wodę. W tym przypadku kwas solny HCl reaguje z wodorotlenkiem potasu KOH. Pierwszym produktem tej reakcji jest oczywiście woda. Natomiast drugi z produktów tej reakcji jest solą. Jednak jaka sól to będzie? Sole są grupą związków o budowie jonowej – w ich skład wchodzą kationy metalu oraz aniony reszt kwasowych. Znajdźmy więc w powyższej reakcji obie z tych rzeczy. Gdy wodorotlenek potasu dysocjuje, uwalnia kationy potasu oraz aniony wodorotlenkowe, natomiast w wyniku dysocjacji kwasu solnego powstają kationy wodorowe oraz aniony chlorkowe. Możesz zauważyć, że kationami metalu są kationy potasu, natomiast anionami reszty kwasowej są aniony chlorkowe. Zarówno kationy potasu K+ jak i aniony chlorkowe Cl- mają naładowane przeciwnie, ale w tym samym stopniu (K+ - jeden na plusie, Cl- - jeden na minusie). Tworzą więc one sól KCl. Natomiast jony wodorowe i aniony wodorotlenkowe w trakcie reakcji łączą się, tworząc obojętną cząsteczkę wody. Podsumujmy: produktami tej reakcji są KCl oraz H2O, a w takim razie A to KCl i E to H2O (lub odwrotnie). Narysować musisz także schemat modelowy tej reakcji – musisz pamiętać, że HCl oraz KOH są w wodzie zdysocjowane i występują w postaci jonów, które zobrazujesz za pomocą kolorowych kul. Na modelu na zielono przedstawione są aniony Cl-, czerwone kule symbolizują atomy lub jony wodoru (H+), szare kationy potasu K+, natomiast niebieskie atomy tlenu. W wyniku reakcji zobojętniania jony H+ łączą się z jonami OH- tworząc obojętne cząsteczki wody.