PH3:
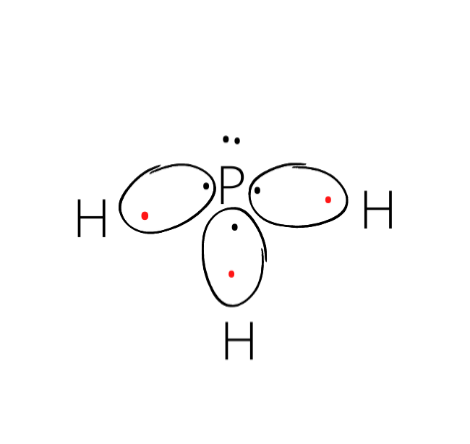
Cząsteczka trygonalna
H2S:
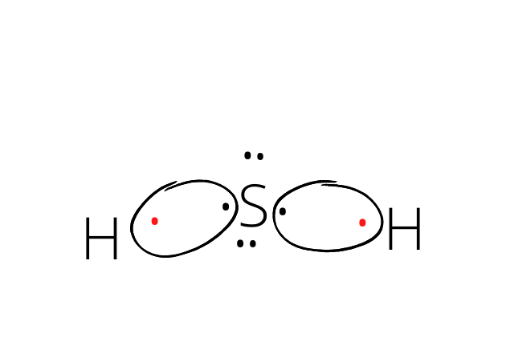
Cząsteczka V-kształtna
SiH4:
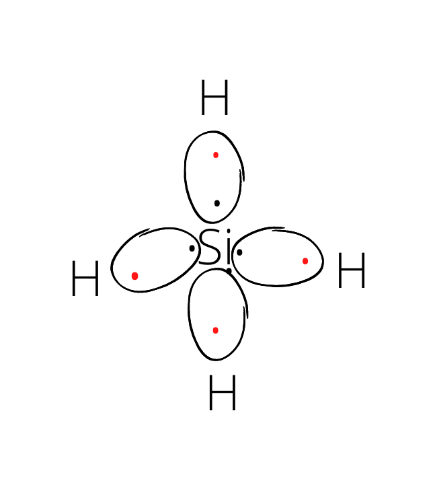
Cząsteczka tetraedryczna
CO2:
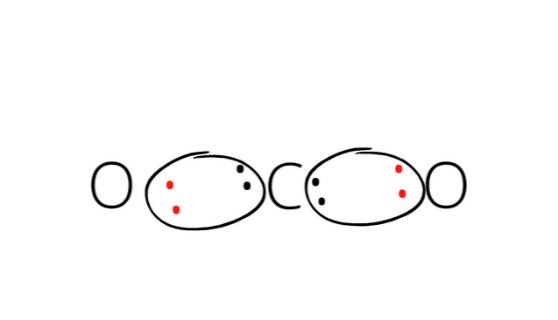
Cząsteczka diagonalna (liniowa)

Teoria VSEPR zakłada, że takie wiążące pary elektronowe odpychają się wzajemnie i dążą do tego, aby znaleźć się możliwie najdalej od siebie, co z kolei decyduje o ostatecznym ułożeniu wiązań względem siebie.