Skrócony wzór strukturalny cząsteczki aldehydu octowego (acetaldehydu, etanalu) można zapisać jako CH3-CHO. Wykonaj polecenia w zeszycie.
a)
Kropkowy wzór elektronowy aldehydu octowego:
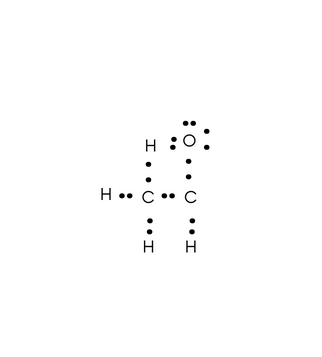
Rozszerzony wzór strukturalny aldehydu octowego:
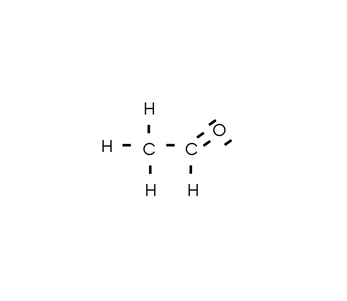
b)
Wiążące pary elektronowe – 7
Niewiążące pary elektronowe - 2
c)
Hybrydyzacja atomów węgla w CH3 – sp3
Hybrydyzacja atomów węgla w C=O – sp2
Hybrydyzacja tlenu – sp2.
d)
Wielkość katów pomiędzy każdą para wiązań:
- pomiędzy C-H w wiązaniu w CH3 – 109,5⁰C
- pomiędzy C-C w wiązaniu CH3 – 109,5⁰C
- pomiędzy C-C w wiązaniu C=O – 120⁰C
- pomiędzy C-H w grupie aldehydowej -CHO – 120⁰C
e)
Wiązania są silnie spolaryzowane: między atomem węgla a atomem tlenu.
Wiązania słabo spolaryzowane (niespolaryzowane): między atomem węgla i wodoru, między atomami węgla,
f) Oddziaływania pomiędzy cząsteczkami w stanie ciekłym – oddziaływania dipol-dipol,
g) Oddziaływania jakie występują pomiędzy cząsteczkami aldehydu octowego a cząsteczkami wody – wiązanie wodorowe.
h) Uzasadnij różnice pomiędzy temperatura wrzenia aldehydu octowego a temperaturami wrzenia innych związków podanymi poniżej.
| Nazwa | Skrócony wzór strukturalny | Masa cząsteczkowa [u] | Temperatura wrzenia [⁰C] |
| aldehyd octowy (etanal) | CH3CHO | 44 | +20 |
| propan | CH3CH2CH3 | 44 | -42 |
| aldehyd propionowy (propanal) | CH3CH2CHO | 58 | +48 |
- Aldehyd octowy i propan mają podobną masę. Różnica pomiędzy aldehydem octowym a propanem wynika z rodzaju oddziaływań dyspersyjnych, aldehyd octowy może dodatkowo tworzyć oddziaływania dipol-dipol, tym samym zwiększa energię potrzebną do zmiany stanu skupienia.
- Różnica pomiędzy aldehydem octowym a aldehydem propionowym wynika z różnej masy. Aldehyd propionowy ma większą masę, więc potrzeba więcej energii potrzebnej do zmiany stanu skupienia.
