Temperaturę przestawiamy w skali Kelvina i obliczamy wartości
![]() . Następnie logarytmujemy wartości stałej szybkości reakcji.
. Następnie logarytmujemy wartości stałej szybkości reakcji.
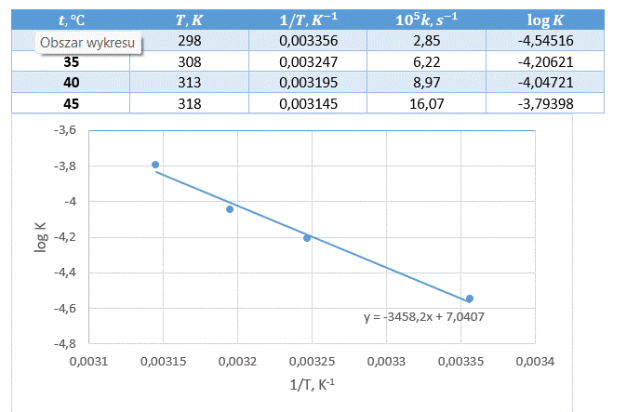
Z nachylenia prostej obliczamy wartość energii aktywacji:
![]() stąd
stąd
![]()
Odpowiedź: Energia aktywacji badanej reakcji wynosi 66 kJ/mol.

Temperaturę przestawiamy w skali Kelvina (pamiętając, że
![]() ) i obliczamy wartości
) i obliczamy wartości
![]() . Następnie logarytmujemy wartości stałej szybkości reakcji. Wyniki umieszczamy w tabeli.
. Następnie logarytmujemy wartości stałej szybkości reakcji. Wyniki umieszczamy w tabeli.
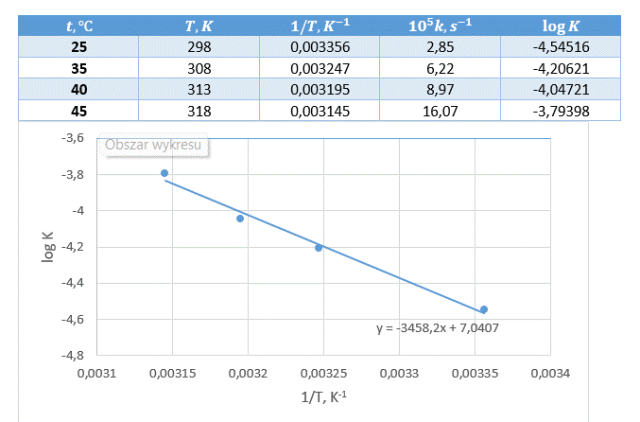
Szkicujemy wykres, umieszczając na osi X – 1/T, a na osi Y – log K. Wyznaczamy równanie prostej.
Z nachylenia prostej obliczamy wartość energii aktywacji, bazując na równaniu Arrheniusa:
![]()
Nachylenie prostej jest równe wartości
![]() .
.
Uwzględniając powyższe dane, obliczamy:
![]() stąd
stąd
![]()
Uzyskana wartość to energia aktywacji badanej reakcji.
