![]()
![]()
![]()
Odpowiedź: Podczas spalania 1 mola metanu wydziela się ok. 810 kJ energii.

Obliczamy nakład energii niezbędny do przeprowadzenia 1 mola metanu i 2 moli tlenu (
![]() ) do postaci wolnych atomów. W tym celu muszą zostać zerwane cztery mole wiązań C
) do postaci wolnych atomów. W tym celu muszą zostać zerwane cztery mole wiązań C
![]() H i dwa mole podwójnych wiązań O
H i dwa mole podwójnych wiązań O
![]() O. (Wiązania w cząsteczkach O₂ nie są typowymi wiązaniami podwójnymi – patrz rozdział 2. – ale energia ich dysocjacji odpowiada takiej uproszczonej strukturze).
O. (Wiązania w cząsteczkach O₂ nie są typowymi wiązaniami podwójnymi – patrz rozdział 2. – ale energia ich dysocjacji odpowiada takiej uproszczonej strukturze).
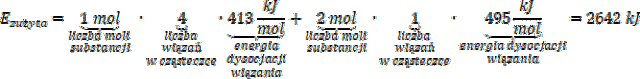
W analogiczny sposób możemy obliczyć wartość energii wydzielanej podczas tworzenia się wiązań w jednym molu
![]() , i dwóch molach
, i dwóch molach
![]() . W tych cząsteczkach występują dwa podwójne wiązania C
. W tych cząsteczkach występują dwa podwójne wiązania C
![]() O i dwa wiązania O
O i dwa wiązania O
![]() H.
H.
![]()
Jak widać, energia wydzielona ma wyższą wartość niż zużyta i zysk energetyczny wynosi:
![]()
Zatem 808 kJ to ilość energii, która wydziela się podczas spalania 1 mola metanu.
