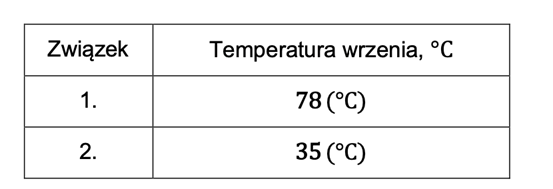

· Etanol (CH₃CH₂OH) ma wyższą temperaturę wrzenia (78 °C), ponieważ grupa –OH tworzy silne wiązania wodorowe między cząsteczkami, co zwiększa energię potrzebną do przejścia w stan gazowy.
· Etanodiol (CH₃CH₂SH) ma niższą temperaturę wrzenia (35 °C), ponieważ siarka tworzy słabsze wiązania wodorowe lub ich brak, a siarkowodorowe oddziaływania są mniej efektywne niż tlenowe.
Wiązanie wodorowe to specyficzny rodzaj oddziaływania międzycząsteczkowego, który powstaje, gdy atom wodoru jest kowalencyjnie związany z silnie elektroujemnym pierwiastkiem, takim jak tlen, azot lub fluor, i jednocześnie oddziałuje z wolną parą elektronową innego elektroujemnego atomu w sąsiedniej cząsteczce.
Dzięki wiązaniom wodorowym cząsteczki mogą tworzyć sieci, co wpływa na właściwości fizyczne substancji, takie jak wyższe temperatury wrzenia i topnienia.