Potrzebne odczynniki:
· Metaliczna miedź,
· Kwas solny (30%),
· Kwas azotowy(V) (30%),
· Roztwór NaOH.
Schemat:
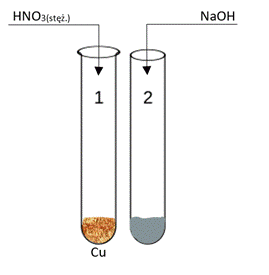
Sposób wykonania:
W probówce z odrobiną metalicznej miedzi dodajemy kroplami roztwór kwasu azotowego(V). Po chwili dodajemy roztwór wodorotlenku sodu. Powstały osad odsączamy na lejku szklanym z wilgotnym sączkiem, aż do uzyskania na sączku osadu. Otrzymany osad umieszczamy w probówce i poddajemy działaniu temperatury w łaźni wodnej.
Obserwacje:
Po dodaniu do metalicznej miedzi stężonego kwasu azotowego(V) obserwujemy wydzielanie się brunatnego gazu. Po dodaniu do uzyskanej substancji wodorotlenku sodu wytrąca się niebieski, galaretowaty osad. Po poddaniu osadu działaniu temperatury obserwujemy zmianę zabarwienia osadu na czarną.
Wnioski:
W pierwszym kroku powstaje azotan(V) miedzi(II) oraz brunatny, trujący gaz tlenku azotu(IV). Następnie po dodaniu NaOH obserwujemy wydzielenie się niebieskiego osadu pochodzącego od wodorotlenku miedzi(II). Wodorotlenek poddajemy działaniu wysokiej temperatury, co prowadzi do rozkładu substancji na czarny osad tlenku miedzi(II).
Równania reakcji chemicznych:
1.
![]()
2.
![]()
3.
![]()

Miedź reaguje ze stężonym kwasem azotowym(V), nie reaguje natomiast z kwasami nieutleniającymi takimi jak kwas solny.