Atomy pierwiastka chemicznego X tworzą jony
X2+ o następującej konfiguracji elektronowej: 1s22s22p63s23p63d10.
Konfiguracja elektronowa atomu X: 1s22s22p63s23p64s23d10 – łączna liczba elektronów = 30
a) Symbol pierwiastka chemicznego X – Zn.
b) Określ położenie tego pierwiastka chemicznego w układzie okresowym – grupa 12, okres 4.
c) Określ, do jakiego bloku konfiguracyjnego należy ten pierwiastek chemiczny – d.
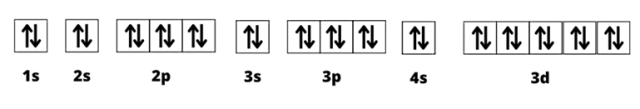
d) Zapisz konfigurację elektronową atomu pierwiastka chemicznego X za pomocą schematu klatkowego.
e) Podaj wartości liczb kwantowych n, l, m, ms opisujących stan elektronów podpowłoki 4s w tym atomie.

1 elektron:
n = 4
l = 0
m = 0
ms =
![]()
2 elektron:
n = 4
l = 0
m = 0
ms = -
![]()

Na podstawie konfiguracji elektronowej pierwiastka chemicznego możemy określić liczbę elektronów. Wiemy, że liczba elektronów jest równa liczbie protonów, czyli liczbie atomowej Z. Na podstawie liczby atomowej Z możemy określić położenie pierwiastka chemicznego w układzie okresowym pierwiastków chemicznych.
n – główna liczba kwantowa, określa energię elektronu w atomie, przyjmuje wartości kolejnych liczb naturalnych: n = 1, 2, 3, 4…
l – poboczna liczba kwantowa, określa kształt orbitali atomowych, przyjmuje wartości całkowite 0 < l < (n – 1),
m – magnetyczna liczba kwantowa, określa liczbę poziomów orbitalnych związanych z ułożeniem orbitali atomowych w przestrzeni pod wpływem zewnętrznego pola magnetycznego.
ms – magnetyczna spinowa liczba kwantowa, określa spin, czyli własny moment pędu elektronu (kierunek obrotu wokół własnej osi). Przyjmuje wartości:
![]() lub -
lub -
![]() .
.