Pierwiastek chemiczny X w stanie podstawowym ma następującą konfigurację elektronową:
1s22s22p63s23p64s23d5 – liczba elektronów: 25 – mangan (Mn).
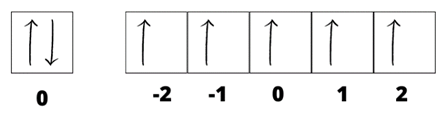
a) Rozmieszczenie elektronów walencyjnych w atomie tego pierwiastka chemicznego w postaci schematu klatkowego:
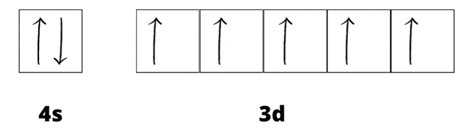
b) Ponumeruj na schemacie klatkowym elektrony od 1 do 7. Opisz stan kwantowy elektronów oznaczonych numerami 3, 5, 6 i podaj wartości liczb kwantowych.
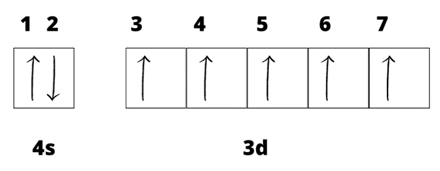
Elektron nr 3: (3d)
n = 3
l = 2
m = -2
ms =
![]()
Elektron nr 5: (5d)
n = 3
l = 2
m = 0
ms =
![]()
Elektron nr 6: (6d)
n = 3
l = 2
m = 1
ms =
![]()
c)
Symbol pierwiastka chemicznego X: Mn,
Skrócony zapis konfiguracji elektronowej jego atomu: [Ar] 4s23d5

Określenie wartości m: