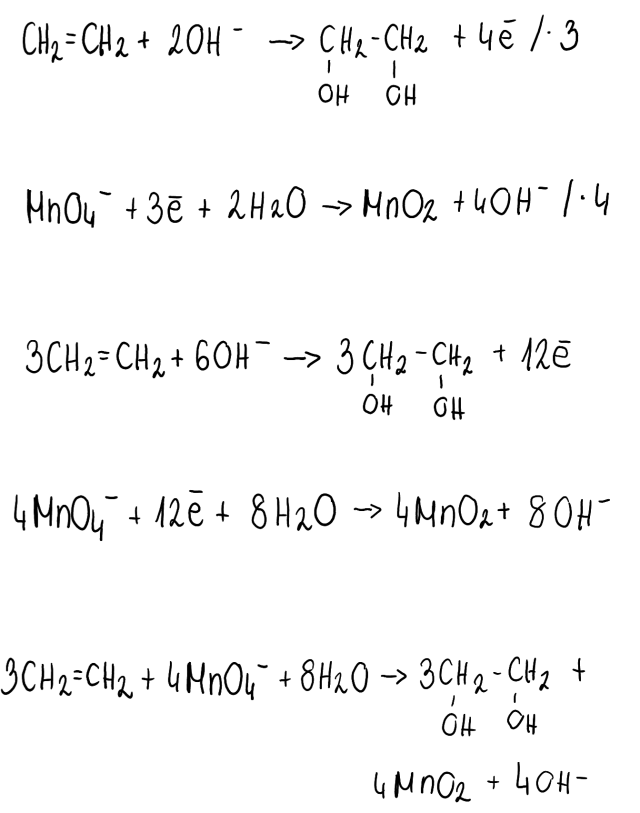

REDUKCJA:
1. W pierwszej kolejności należy ustalić, że redukcji ulega mangan, tworząc jony, w których występuje na stopniach utleniania +VII po stronie substratów i +IV po stronie produktów.
2. Aby wyrównać różnicę w stopniach utlenienia, należy dodać odpowiednią ilość elektronów po jednej ze stron- w tym przypadku po stronie substratów należy dopisać 3 elektrony.
3. Różnice w ładunkach po obu stronach równania, w związku z tym, iż mamy do czynienia ze środowiskiem zasadowym (OH- w produktach), wyrównujemy za pomocą jonów wodorotlenkowych- dopisujemy ich po stronie produktów 4.
4. Różnice w ilości tlenów i wodorów po obu stronach równania wyrównujemy, dodając po odpowiedniej stronie konkretną liczbę moli atomów wody- w tym wypadku 2 mole wody po stronie substratów.
UTLENIANIE
1. Ustalamy, że utlenianiu ulega eten, tworząc etanodiol. W etenie stopień utlenienia atomu węgla wynosi -II, a w etanodiolu- 0.
2. Aby wyrównać różnicę w stopniach utlenienia, należy dodać odpowiednią ilość elektronów po jednej ze stron- 4 elektrony po stronie produktów.
3. Różnice w ładunkach po obu stronach równania, w związku z tym, iż mamy do czynienia ze środowiskiem zasadowym (OH- w produktach), wyrównujemy za pomocą jonów wodorotlenkowych- dopisujemy ich po stronie substratów 2.
UZGADNIANIE REAKCJI KOŃCOWEJ
1. W obu równaniach ilości elektronów są różne, w związku z czym trzeba przemnożyć je w taki sposób, aby wówczas te ujemne cząstki były w obu równaniach równe. W tym celu całe równanie reakcji utleniania mnożymy przez 3, a redukcji- przez 4.
2. Jeśli istnieje taka potrzeba, należy skrócić cząsteczki wody i jony wodorotlenkowe, które powtarzają się po przeciwnych stronach równań.