Niezbędny sprzęt i odczynniki: kolba, łuczywo i źródło ognia, kauczuk chloroprenowy, azotan(V) srebra(I), wężyk do zbierania gazu, probówka z korkiem, uniwersalny papierek wskaźnikowy.
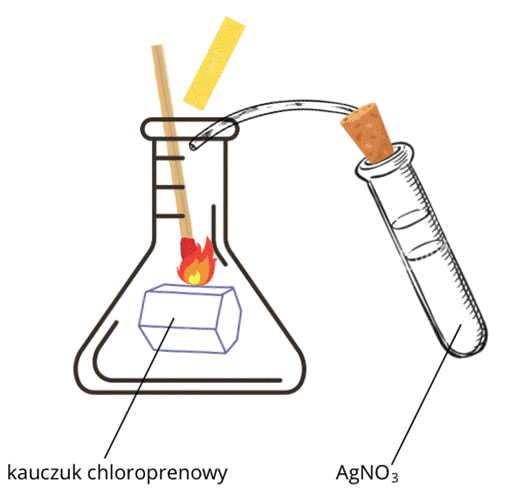
Przebieg doświadczenia: W kolbie należy umieścić próbkę kauczuku chloroprenowego. U wylotu kolby umieszczamy wężyk do zbierania gazu, który odprowadzi go do probówki z AgNO3. Dodatkowo nad kolbą umieszczamy uniwersalny papierek wskaźnikowy. Próbkę kauczuku chloroprenowego podpalamy przy pomocy tlącego się łuczywka.
Obserwacje: W wyniku spalenia próbki kauczuku chloroprenowego w probówce pojawił się osad. Uniwersalny papierek wskaźnikowy barwi się na czerwono pod wpływem wydzielanego gazu.
Wnioski: Podczas spalania kauczuku chloroprenowego wydziela się chlorowodór o odczynie kwasowym. W probówce powstał osad – chlorek srebra(I).
Równanie reakcji: AgNO3 + HCl → AgCl + HNO3

Zastanów się nad metodą wykrywania chlorowodoru. Jest to gaz o odczynie kwasowym, więc barwi uniwersalny papierek wskaźnikowy na czerwono. Jednak nie jest to jedyna taka substancja. Należy przygotować doświadczenie, którego wynik jednoznacznie pozwoli określić, że wydzielanym gazem jest chlorowodór.
Spójrz do tabeli rozpuszczalności soli. W wyniku reakcji chlorowodoru z azotanem(V) srebra(I) powstaje osad – chlorek srebra. Zatem, aby udowodnić obecność HCl, należy poddać HNO3 działaniu tego gazu.