Czynniki elektrofilowe to drobiny o charakterze kwasów Lewisa, czyli drobiny z luką elektronową (deficytem elektronów). Mogą one przyjąć elektrony od związków będących zasadami Lewisa, czyli od czynników nukleofilowych.
Do czynników elektrofilowych zaliczamy: H3O+, H+, (C33)2CH+, GaCl3, Cl∙.

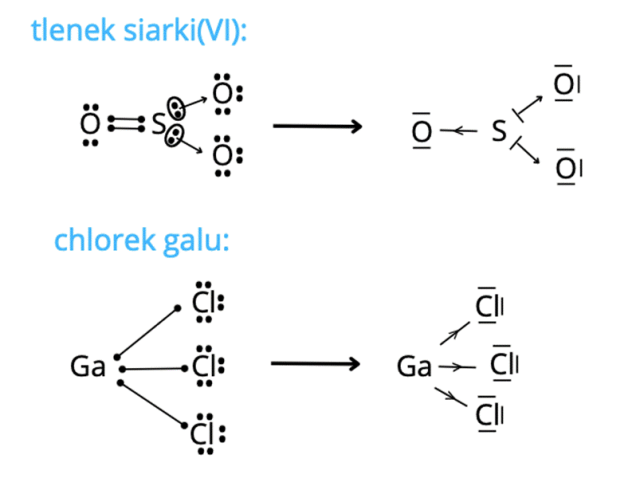
Aby rozwiązać to zadanie, należy przypomnieć sobie, jak definiujemy kwasy Lewisa. Są to związki, którym, najprościej mówiąc, brakuje elektronów. Rozpoznajemy je zawsze dzięki dodatnim indeksom górnym. Kwasami Lewisa są też rodniki, które posiadają niesparowane elektrony. W przypadku GaCl3 i SO3. należy spojrzeć na wzory elektronowe. W tlenku siarki(VI) tworzą się wiązania koordynacyjne spolaryzowane, co powoduje, że wszystkie atomy zyskują oktet elektronów. Natomiast w chlorku galu, mimo utworzenia trzech wiązań z atomami chloru, atom galu wciąż nie ma oktetu. Występuje tutaj luka elektronowa.