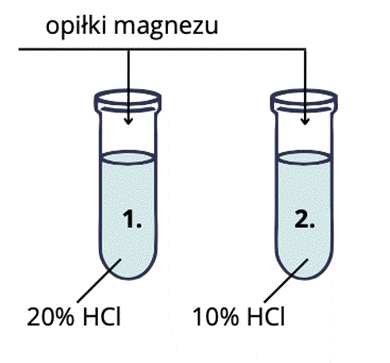
Sprzęt i odczynniki: dwie probówki, opiłki magnezu, kwas solny w stężeniu 10% i 20%.
Obserwacje: W probówce pierwszej opiłki magnezu rozpuszczają się szybciej niż w probówce drugiej. W probówce pierwszej szybciej dochodzi do wydzielenia pęcherzyków gazu niż w probówce drugiej.
Wnioski: Wzrost stężenia substratu powoduje wzrost szybkości reakcji chemicznej.

Stężenie substratów maleje w trakcie przebiegu reakcji. Powoduje to, że liczba zderzeń cząstek maleje, a co za tym idzie – maleje szybkość reakcji. Wyższe stężenie zapewnia zwiększoną liczbę zderzeń cząstek.
Reakcja zachodzi zgodnie z równaniem: Mg + 2HCl → MgCl2 + H2 – wydzielającym się gazem jest wodór.