RKNO3 = 170 g / 100 g H2O w 80 °C
mr = 170 g + 100 g
mr = 270 g
270 g ---- 170 g KNO3
200 g ----- x g KNO3
x =
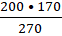
x = 126 g KNO3
RKNO3 = 30 g / 100 g H2O w 20 °C
mr = 30 g + 100 g
mr = 130 g
30 g KNO3 ----- 130 g roztworu
y g KNO3 ----- 200 g roztworu
y =
![]()
y = 46 g KNO3
m = 126 g – 46 g
m = 80 g
Odpowiedź: Masa odsączonych i wysuszonych kryształów wynosi 80 g.

W pierwszym kroku sprawdź na krzywej rozpuszczalności, jaką rozpuszczalność ma ta sól w temperaturze 80 °C. Oblicz masę roztworu nasyconego.
RKNO3 = 170 g / 100 g H2O w 80 °C
mr = 170 g + 100 g
mr = 270 g
Następnie oblicz, za pomocą metody proporcji, ile azotanu(V) potasu znajduje się w roztworze o masie 200 g. Jako „x” oznacz masę wody. Wartości znajdujące się po przekątnej względem siebie pomnóż, a wartość po przekątnej względem „x” wstaw do mianownika ułamka.
270 g ---- 170 g KNO3
200 g ----- x g KNO3
x =
![]()
x = 126 g KNO3
W kolejnym kroku sprawdź na krzywej rozpuszczalności, jaką rozpuszczalność ma ta sól w temperaturze 20 °C. Oblicz masę roztworu nasyconego.
RKNO3 = 30 g / 100 g H2O w 20 °C
mr = 30 g + 100 g
mr = 130 g
Następnie oblicz, za pomocą metody proporcji, ile maksymalnie azotanu(V) potasu może się znajdować w roztworze o masie 200 g w temperaturze 20 °C. Jako „x” oznacz masę wody. Wartości znajdujące się po przekątnej względem siebie pomnóż, a wartość po przekątnej względem „x” wstaw do mianownika ułamka.
30 g KNO3 ----- 130 g roztworu
y g KNO3 ----- 200 g roztworu
y =
![]()
y = 46 g KNO3
Odejmij od masy azotanu(V) potasu w roztworze w temperaturze 80 °C masę azotanu(V) potasu w roztworze w temperaturze 20 °C.
m = 126 g – 46 g
m = 80 g
Sformułuj odpowiedź.