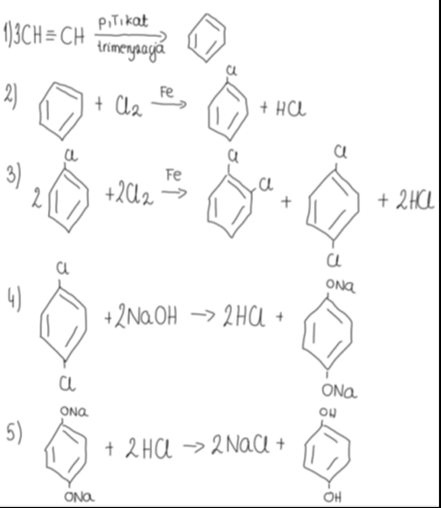
Cząsteczka związku powstałego w reakcji nr 3 ma wypadkowy moment dipolowy równy zero.

Moment dipolowy to wielkość fizyczna, która opisuje rozkład ładunków elektrycznych w cząsteczce. Jest to wektor, którego kierunek wskazuje od ładunku dodatniego do ujemnego, a wartość zależy od wielkości ładunków oraz odległości między nimi.
Moment dipolowy jest szczególnie ważny w chemii, ponieważ pozwala określić, czy cząsteczka jest polarna, czyli czy posiada rozdzielony ładunek (część cząsteczki jest częściowo naładowana dodatnio, a część ujemnie). Cząsteczki polarne mają niezerowy moment dipolowy, natomiast cząsteczki apolarne (np. cząsteczki jednorodne, takie jak O₂ czy N₂) mają moment dipolowy równy zeru.
Przykładowe równania zachodzących reakcji: