Vo = 0,002 cm3
0,002 cm3 = 0,000002 dm3
d =
![]() / • V
/ • V
mo = d • V
mo = 1,43 g/dm3 • 0,000002 dm3
mo = 0,00000286 g
masy cząsteczkowe:
mO = 16 g
mHgO = 201 g + 16 g
mHgO = 217 g
2HgO → 2Hg + O2
434 g HgO --------- 32 g O2
X g HgO --------- 0,00000286 g O2
X = 0,0000388 g
Odpowiedź: W reakcji analizy tlenku rtęci(II) wzięło udział 0,0000388 g tlenku rtęci(II).

W pierwszym kroku zamień jednostkę objętości z cm3 na dm3.
Vo = 0,002 cm3
0,002 cm3 = 0,000002 dm3
Następnie oblicz masę otrzymanego tlenu. Skorzystaj ze wzoru na gęstość. Pomnóż stronami przez objętość.
d =
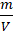 / • V
/ • V
mo = d • V
mo = 1,43 g/dm3• 0,000002 dm3
mo = 0,00000286 g
Oblicz masę cząsteczkową tlenku rtęci(II). Stwórz proporcję. Jako „X” oznacz masę tlenku rtęci(II), jaką wykorzystano do reakcji. Oblicz proporcję mnożąc wartości znajdujące się po przekątnej względem siebie. Wartość naprzeciwko „X” wstaw do mianownika równania.
mHgO = 201 g + 16 g
mHgO = 217 g
2HgO → 2Hg + O2
434 g HgO --------- 32 g O2
X g HgO --------- 0,00000286 g O2
X = 0,0000388 g
Sformułuj odpowiedź.