3 Cd + 2 Fe3+→ 3 Cd2+ + Fe
Fe – 56
![]()
Cd – 112
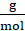
3 Cd – 2 Fe
3 ∙ 112
![]() → 2 ∙ 56
→ 2 ∙ 56
![]()
X → 168 mg
X =
![]() = 504 mg
= 504 mg
Masa elektrody kadmowej spadła o 504 mg.

Z równania reakcji wymiany elektronów układamy proporcję, posługując się masami molowymi oraz zadaną ∆m dla żelaza. Wyliczamy z proporcji, że masa drugiej elektrody zmienia się o 504 mg. Ponieważ jest to elektroda kadmowa stanowiąca anodę, będzie ona przechodzić do roztworu w formie jonów, znaczy, że jej masa będzie maleć podczas pracy ogniwa.