Stan początkowy (przed dodaniem A)
Reakcja:
![]()
Początkowo:
![]() ,
,
![]() ,
,
![]() ,
,
![]()
Niech w stanie równowagi powstanie
![]() mola produktu:
mola produktu:
·
![]()
·
![]()
·
![]()
·
![]()
Stała równowagi:
![]()
![]()
![]()
![]()
Dodanie 2 moli A
Nowe ilości (tuż po dodaniu, przed przesunięciem równowagi):
·
![]()
·
![]()
·
![]()
·
![]()
Nowa równowaga
Niech reakcja przesunie się w prawo o
![]() :
:
·
![]()
·
![]()
·
![]()
·
![]()
Stała równowagi:
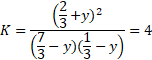
Po rozwiązaniu:
![]()
Nowa ilość C:
![]()
Zmiana liczby moli
![]()
Liczba moli produktu C zwiększy się o 0,33 mola.

Stała równowagi (Kc) to wielkość, która opisuje stan równowagi chemicznej reakcji odwracalnej i informuje, w jakim stopniu reagenty przekształcają się w produkty. Jest ona równa ilorazowi iloczynu stężeń produktów do iloczynu stężeń substratów, przy czym każde stężenie podnosi się do potęgi odpowiadającej współczynnikowi stechiometrycznemu w równaniu reakcji.
Dla reakcji ogólnej: aA + bB⇄cC + dD, stała równowagi ma postać:
![]() .
.
Obliczanie zadań polega najczęściej na kilku krokach: najpierw zapisujesz równanie reakcji i wzór na K, potem podstawiasz dane stężenia (równowagowe, nie początkowe), a jeśli ich nie znasz, tworzysz tzw. tabelkę zmian stężenia: początkowe – zmiana – równowagowe), gdzie oznaczasz zmiany stężeń np. jako x i wyrażasz wszystkie stężenia w stanie równowagi przez x, następnie podstawiasz to do wzoru na K i rozwiązujesz równanie, często kwadratowe. Na końcu sprawdzasz, czy wynik ma sens (np. stężenia nie mogą być ujemne).
