Równanie kinetyczne nie jest zgodne ze stechiometrią reakcji.Całkowity rząd reakcji wynosi 3.Jednostką stałej szybkości reakcji jest dm6 · mol-2 · s-1.Dwukrotne zwiększenie stężenia anionów jodkowych bez zmiany stężenia kationów żelaza(III) spowoduje 4-krotny wzrost szybkości reakcji.W celu 4-krotnego zmniejszenia szybkości reakcji bez zmiany stężenia anionów jodkowych należy 4-krotnie zmniejszyć stężenie jonów żelaza(III).

![]()
rząd względem
![]() = 1, rząd względem
= 1, rząd względem
![]() = 2, zatem całkowity rząd =
= 2, zatem całkowity rząd =
![]() .
.
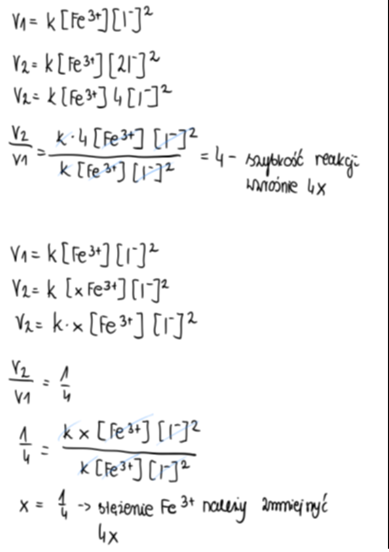
Stosunek
![]() pozwala odpowiedzieć na pytanie, jak (czy wzrośnie czy zmaleje) i ilu krotnie zmieni się szybkość danej reakcji.
pozwala odpowiedzieć na pytanie, jak (czy wzrośnie czy zmaleje) i ilu krotnie zmieni się szybkość danej reakcji.
