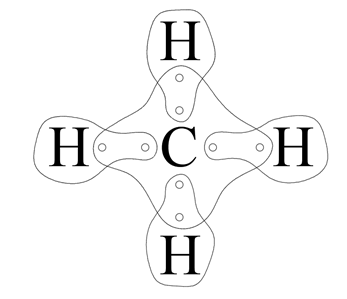
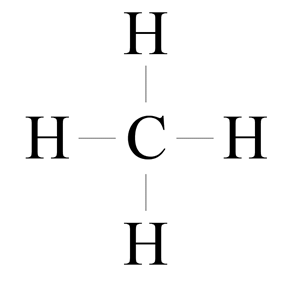
Wodór ma jeden elektron walencyjny. Węgiel ma cztery elektrony walencyjne.

Atom wodoru dąży do uzyskania dubletu elektronowego. Brakuje mu do tego jednego elektronu. Atomowi węgla brakuje czterech elektronów do uzyskania oktetu elektronowego. węgiel brakujące cztery elektrony uwspólnia z czterema atomami wodoru. Mamy cztery wspólne pary elektronowe (cztery wiązania pojedyncze).
Różnica elektroujemności:
![]() – wiązanie kowalencyjne spolaryzowane
– wiązanie kowalencyjne spolaryzowane

Jeśli różnica elektroujemności (oznaczonej czerwonymi cyframi w układzie okresowym na tyle okładki) jest mniejsza niż 1,7, pierwiastki tworzą równanie kowalencyjne. Jeśli różnica ta mieści się w przedziale 0-0,4, mamy do czynienia z wiązaniem kowalencyjnym niespolaryzowanym, gdy powyżej- kowalencyjnym spolaryzowanym. Jeśli jednak różnica ta wynosiłaby 1,7 i więcej- wiązanie między atomami ma charakter jonowy.
Różnica elektroujemności zawsze jest wartością nieujemną- od wartości większej odejmujemy mniejszą, niezależnie od kolejności występowania pierwiastków we wzorze.