Dipol jest układem dwóch różnoimiennych (a więc dodatniego i ujemnego) ładunków. Wytwarzają one tzw. moment dipolowy na dwóch krańcach cząsteczki.
Cząsteczka polarna jest cząsteczką, która przede wszystkim posiada wiązanie kowalencyjne spolaryzowane w swojej strukturze. To właśnie w niej elektrony przesunęły się w jedną ze stron.
W cząsteczce HI łączą się ze sobą jod i wodór. Jod ma siedem elektronów walencyjnych, a wodór ma jeden. Aby uzyskać dublet elektronowy, wodór potrzebuje jeszcze jednego elektronu. Aby uzyskać oktet elektronowy, jod również potrzebuje jednego dodatkowego elektronu, zatem uwspólnia go z wodorem. Tworzy się jedna wspólna para elektronowa (mamy wiązanie pojedyncze), dodatkowo na atomie jodu pozostaje jeszcze 6 niezwiązanych z wodorem elektronów, tworzących 3 wolne pary elektronowe.
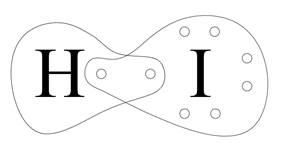
W cząsteczkach, które tworzone są przez różne pierwiastki niemetaliczne, wspólna para elektronowa przesunięta jest w stronę atomu o wyższej elektroujemności. Wodór ma elektroujemność 2,1 a jod 2,5. Zatem atom jodu mocniej przyciąga wspólną parę elektronową. Jest to polaryzacja wiązania chemicznego, w wyniku czego powstaje cząsteczka, która jest dipolem (ma biegun dodatni i ujemny).

Z momentem dipolowym mamy do czynienia, kiedy dochodzi do nierównomiernego (niesprawiedliwego J ) rozkładu elektronów w cząsteczce. Pierwiastek bardziej elektroujemny będzie mieć w swoim otoczeniu większą gęstość elektronów, zaś ten o niższej elektroujemności- mniejszą gęstość.