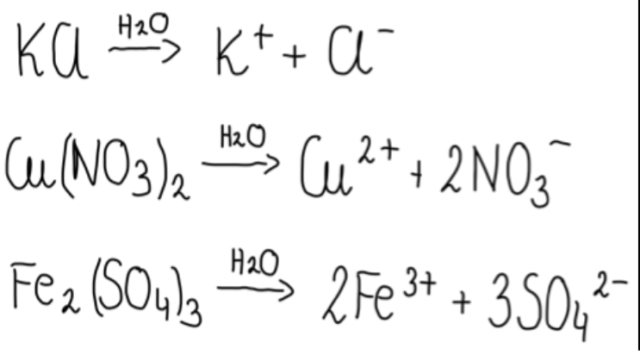

Dysocjacja elektrolityczna związków o wiązaniu jonowym polega na rozpadzie ich cząsteczek na jony dodatnie (kationy) i ujemne (aniony) podczas rozpuszczania w wodzie.
Związki o wiązaniu jonowym zbudowane są z dodatnich i ujemnych jonów, które w stanie stałym tworzą sieć krystaliczną. Gdy taki związek zostanie wprowadzony do wody:
· Cząsteczki wody otaczają jony – działa tu siła przyciągania między cząsteczkami wody (dipolami) a jonami.
· Woda osłabia siły elektrostatyczne między jonami w sieci krystalicznej.
· Jony oddzielają się od siebie i przechodzą do roztworu jako swobodne jony.
· Powstały roztwór przewodzi prąd elektryczny, ponieważ zawiera swobodne jony.