α > 5%
K =
![]() / *(
/ *(
![]()
K
![]() =
=
![]() /
/
![]()
C =
![]() =
=
![]() = 0,018
= 0,018
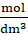
HR + H2O ↔ H3O+ + R-
0,018
![]() ∙ 10% = 0,0018
∙ 10% = 0,0018
![]()

Stężenie jonów oksoniowych powstałych w wyniku dysocjacji możemy obliczyć, znając prawo rozcieńczeń Ostwalda. Nie możemy zastosować jego uproszczonej wersji, ponieważ α > 5%. Przekształcamy wzór tak, aby wyliczyć z niego niewiadomą C (stężenie roztworu). Mając stopień dysocjacji i całkowite stężenie możemy wymnożyć je przez siebie, otrzymując poszukiwane stężenie jonów oksoniowych. Z równania dysocjacji widzimy, że stężenie kwasu i jonów oksoniowych będzie w takiej samej proporcji 1:1 przez ich stosunek molowy.