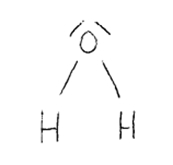
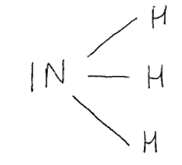
NH3, H2O – zasada
H+ – kwas

Kwasy w myśl teorii Lewisa są indywiduami będącymi akceptorem pary elektronowej. Kation H+ nie ma elektronów na swojej powłoce walencyjnej, więc łącząc się w związki, będzie przyjmował elektrony (pary elektronowe). Zasada jest natomiast donorem pary elektronowej, więc związek mający wolną parę elektronową w swojej strukturze będzie zasadą (NH3 i H2O spełniają to założenie). Elektronowe cząsteczki wody i amoniaku: