Oblicz skład procentowy mieszaniny poreakcyjnej.
13,5% Fe, 86,5% FeO

Reakcja przebiega w 2 etapach:
![]()
![]()
Ilość użytego CO:
1 mol – 0,0224 m3
x moli – 89,6 m3
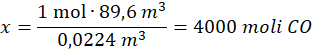
3 kilomole Fe2O3 = 3000 moli
Reakcja 1.
Fe2O3 i CO reagują w stosunku 1 : 1 – na 3000 moli Fe2O3 zostaną zużyte 3000 moli CO, powstanie 6000 moli FeO, zostanie 1000 moli CO do wykorzystania w reakcji 2.
Reakcja 2.
Wykorzystuje 1000 moli CO. FeO i CO reagują w stosunku 1:1, więc zostanie zużyte 1000 moli FeO z 1 reakcji, powstanie 1000 moli Fe.
W mieszaninie końcowej znajduje się 5000 moli FeO (6000-1000 zużyty w reakcji 2) i 1000 moli Fe
Masa mieszaniny:
![]()
Masa FeO w mieszaninie:
![]()
Procent FeO w mieszaninie:
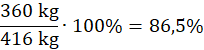
Procent Fe w mieszaninie:
![]()

Ćwiczenie 4.42.
75Ćwiczenie 4.51.
77Ćwiczenie **4.60.
78Ćwiczenie *4.74.
79Ćwiczenie *4.75.
79Ćwiczenie *4.94.
83Ćwiczenie *4.99.
83Ćwiczenie 4.143.
93Ćwiczenie 4.146.
94Ćwiczenie 4.147.
94Ćwiczenie 4.148.
94Ćwiczenie 4.149.
94Ćwiczenie 4.150.
94Ćwiczenie 4.151.
94Ćwiczenie *4.160.
96Ćwiczenie 4.161.
96Ćwiczenie *4.166.
97Ćwiczenie 4.167.
100Ćwiczenie 4.168.
100Ćwiczenie 4.180.
102Ćwiczenie *4.184.
102Ćwiczenie 4.188.
103Ćwiczenie 4.189.
103Ćwiczenie 4.190.
103Ćwiczenie 4.191.
103Ćwiczenie 4.193.
103Ćwiczenie 4.194.
103Ćwiczenie 4.197.
104Ćwiczenie *4.198.
104Ćwiczenie 4.202.
108Ćwiczenie 4.218.
110Ćwiczenie 4.219.
110
