Oblicz ilość MgS powstałą z opisanej mieszaniny.
17,5 g.

![]()
Z równania wiadomo, że 1 mol magnezu – 24 g - reaguje z 1 molem siarki – 32 g. Aby obliczyć nadmiar/niedomiar wybieramy jeden substrat, względem którego policzymy potrzebną stechiometryczną ilość drugiego związku.
Np. Obliczamy ile magnezu przereaguje w tej reakcji z 10 g siarki:
24 g Mg – 32 g S
x g – 10 g
![]()
Z 10 g S przereaguje 7,5 g Mg, więc użyto za dużo magnezu (9 g).
Ilość powstałego produktu zawsze obliczamy względem substratu, którego NIE użyto w nadmiarze – tylko on przeraguje w całości.
Z równania wynika, że z 1 mola siarki – 32 g – powstaje 1 mol MgS – 56 g. Ilość powstała z 10 g siarki:
m MgS – 56 g/mol
32 g S – 56 g MgS
10 g – y
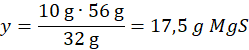

Ćwiczenie 4.42.
75Ćwiczenie 4.51.
77Ćwiczenie **4.60.
78Ćwiczenie *4.74.
79Ćwiczenie *4.75.
79Ćwiczenie *4.94.
83Ćwiczenie *4.99.
83Ćwiczenie 4.143.
93Ćwiczenie 4.146.
94Ćwiczenie 4.147.
94Ćwiczenie 4.148.
94Ćwiczenie 4.149.
94Ćwiczenie 4.150.
94Ćwiczenie 4.151.
94Ćwiczenie *4.160.
96Ćwiczenie 4.161.
96Ćwiczenie *4.166.
97Ćwiczenie 4.167.
100Ćwiczenie 4.168.
100Ćwiczenie 4.180.
102Ćwiczenie *4.184.
102Ćwiczenie 4.188.
103Ćwiczenie 4.189.
103Ćwiczenie 4.190.
103Ćwiczenie 4.191.
103Ćwiczenie 4.193.
103Ćwiczenie 4.194.
103Ćwiczenie 4.197.
104Ćwiczenie *4.198.
104Ćwiczenie 4.202.
108Ćwiczenie 4.218.
110Ćwiczenie 4.219.
110
