Oblicz objętość produktów rozkładu 1 g NH4HCO3 w podanych warunkach.
1,58 dm3

![]()
W reakcji powstają 3 mole produktów gazowych. Obliczamy ich łączna objętość:
Dane:
n – 3 mole
T – 500 K
p –1000 hPa
V - ?
Dane podstawiamy do przekształconego równania Clapeyrona:
![]()
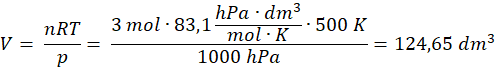
m NH4HCO3 – 79 g/mol
Z 1 mola soli – 79 g – powstaje 124,65 dm3 produktów. Ilość produktów powstała z 1 g soli:
79 g NH4HCO3 – 124,65 dm3 produktów
1 g – x
![]()

Ćwiczenie 4.42.
75Ćwiczenie 4.51.
77Ćwiczenie **4.60.
78Ćwiczenie *4.74.
79Ćwiczenie *4.75.
79Ćwiczenie *4.94.
83Ćwiczenie *4.99.
83Ćwiczenie 4.143.
93Ćwiczenie 4.146.
94Ćwiczenie 4.147.
94Ćwiczenie 4.148.
94Ćwiczenie 4.149.
94Ćwiczenie 4.150.
94Ćwiczenie 4.151.
94Ćwiczenie *4.160.
96Ćwiczenie 4.161.
96Ćwiczenie *4.166.
97Ćwiczenie 4.167.
100Ćwiczenie 4.168.
100Ćwiczenie 4.180.
102Ćwiczenie *4.184.
102Ćwiczenie 4.188.
103Ćwiczenie 4.189.
103Ćwiczenie 4.190.
103Ćwiczenie 4.191.
103Ćwiczenie 4.193.
103Ćwiczenie 4.194.
103Ćwiczenie 4.197.
104Ćwiczenie *4.198.
104Ćwiczenie 4.202.
108Ćwiczenie 4.218.
110Ćwiczenie 4.219.
110
