Schemat doświadczenia:
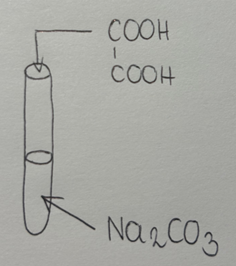
· Obserwacje: Wydziela się bezbarwny, bezwonny gaz.
· Wniosek: Kwas szczawiowy jest mocniejszy od kwasu węglowego.

Aby udowodnić, że jakiś kwas jest słabszy od innego, należy przeprowadzić reakcję kwasu mocniejszego z solą słabszego z nich. Zawsze skutkuje to wyparciem słabszego kwasu z roztworu jego soli.
Kwas szczawiowy jest kwasem mocniejszym od kwasu węglowego. Świadczą o tym wartości stałych dysocjacji dla obu kwasów- owa stała definiuje moc elektrolitu (kwasu, zasady)- im wartość jest wyższa, tym elektrolit mocniejszy.
W doświadczeniu zachodzi reakcja:
COOH-COOH + Na2CO3à H2O + CO2 + COONa-COONa à doszło do wyparcia kwasu węglowego z roztworu jego soli, ale jest to na tyle nietrwała cząsteczka, że od razu rozpada się do wody oraz wydzielającego się dwutlenku węgla