N2 + O2![]()
Objętość reaktora wynosi 1 dm3, dlatego liczby moli traktujemy jako stężenia.
| N2 | O2 | 2 NO | |
| Cpoczątkowe [mol/dm3] | 3 | 3 | 0 |
| ΔC | -x | -x | +2x |
| Crównowagowe [mol/dm3] | 3-x | 3-x | 2x |
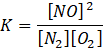
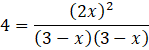
![]()
![]()
![]()
![]()
| N2 | O2 | 2 NO | |
| Cpoczątkowe [mol/dm3] | 1,5+2 | 1,5 | 3 |
| ΔC | -x | -x | +2x |
| Crównowagowe [mol/dm3] | 3,5-x | 1,5-x | 3+2x |
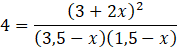
![]()
Stężenia substratów zmaleją o 0,375, a produktu wzrośnie o 0,75.

Na początku zapisz reakcję:
N2 + O2![]()
Objętość reaktora wynosi 1 dm3, dlatego liczby moli traktujemy jako stężenia.
Sporządź tabelę z zależnościami:
| N2 | O2 | 2 NO | |
| Cpoczątkowe [mol/dm3] | 3 | 3 | 0 |
| ΔC | -x | -x | +2x |
| Crównowagowe [mol/dm3] | 3-x | 3-x | 2x |
Oblicz x, korzystając ze stałej równowagi:
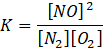
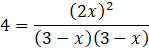
![]()
Oblicz stężenia równowagowe:
![]()
![]()
![]()
Sporządź nową tabelę, uwzględniając w niej nowe stężenia i dodatek 2 moli N2:
| N2 | O2 | 2 NO | |
| Cpoczątkowe [mol/dm3] | 1,5+2 | 1,5 | 3 |
| ΔC | -x | -x | +2x |
| Crównowagowe [mol/dm3] | 3,5-x | 1,5-x | 3+2x |
Oblicz x:
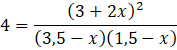
![]()
Stężenia substratów zmaleją o 0,375, a produktu wzrośnie o 0,75.
