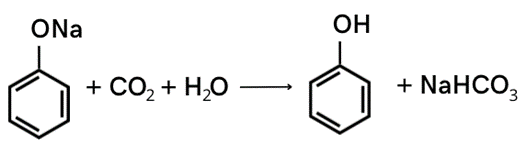
1. Fenolan sodu:
V = 250 cm3
C = 0,1 mol/dm3
0,1 mol — 1000 cm3
x — 250 cm3
x = 0,1 ∙ 250 : 1000 = 0,025 [mol]
2. 1 mol fenolanu sodu — 22,4 dm3
0,025 mol fenolanu sodu — y
y = 0,025 ∙ 22,4 : 1 = 0,56 [dm3]
Odpowiedź: W tej reakcji niezbędne jest 0,56 dm3 tlenku węgla(IV).

Krok 1: Zapisz równanie reakcji.
Krok 2: W zadaniu mamy 250 cm3 fenolanu sodu o stężeniu 0,1 mol/dm3. Na tej podstawie obliczamy ilość moli w naszej objętości substancji. Pamiętaj, że 1 dm3 = 1000 cm3.
0,1 mol — 1000 cm3
x — 250 cm3
x = 0,1 ∙ 250 : 1000 = 0,025 [mol]
Krok 3: Spójrz na wartości stechiometryczne. 1 mol fenolanu sodu reaguje z 1 molem tlenku węgla(IV). 1 mol gazu w warunkach normalnych zajmuje objętość 22,4 dm3. Oblicz objętość tlenku węgla(IV) dla 0,025 mol fenolanu sodu przy pomocy proporcji.
1 mol fenolanu sodu — 22,4 dm3
0,025 mol fenolanu sodu — y
y = 0,025 ∙ 22,4 : 1 = 0,56 [dm3]