Równanie reakcji spalania metanu można opisać w sposób następujący: metan (![]()
![]()
![]()
![]()
Metan, będący czwartym najczęściej występującym gazem w atmosferze, składa się z jednego atomu węgla i czterech atomów wodoru. Podczas spalania metanu, każda cząsteczka metanu reaguje z dwiema cząsteczkami tlenu (które zawsze występują w postaci dwuatomowej, ![]()
Równanie reakcji można zapisać jako:
![]()
Warto zwrócić uwagę, że na spalenie jednej cząsteczki metanu potrzeba dwóch cząsteczek tlenu.
Masy atomów można wyrazić w jednostkach masy atomowej (u). Masa węgla wynosi 12 u, masa wodoru wynosi 1 u, a masa tlenu wynosi 16 u.
Masa cząsteczki metanu (![]()
![]()
![]()
![]()
Masa cząsteczki tlenu dwuatomowego (![]()
![]()
![]()
![]()
Aby obliczyć masę tlenu potrzebną do spalenia 1 kg metanu, możesz skorzystać z proporcji:
![]()
Przemnóż przez ![]()
![]()
![]()
![]()
![]()
Odpowiedź: Do spalenia 1 kg metanu potrzebujesz 4 kg tlenu.
Teraz możesz obliczyć masę powstałych produktów reakcji. Masa substratów (metanu i tlenu) wynosi 5 kg (1 kg metanu + 4 kg tlenu).
Aby obliczyć masę powstałych produktów, możesz użyć równania zmiany energii i masy Einsteina:
![]()
gdzie ![]()
![]()
Zmiana masy substratów wynosi:
![]()
![]()
![]()
gdzie ![]()
![]()
![]()
![]()
![]()
Podstaw wartości:
![]()
![]()
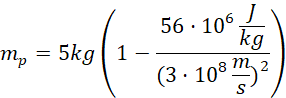
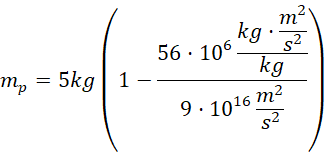
![]()
![]()
Odpowiedź: Masa powstałych produktów reakcji wynosi około 4,99999999689 kg.

Na początek, zapisz równanie reakcji spalania metanu. Metan, który jest głównym składnikiem gazu ziemnego, spala się w obecności tlenu, tworząc dwutlenek węgla i wodę. Zapisz to równanie:
![]()
Teraz możesz obliczyć, ile tlenu jest potrzebne do spalenia 1 kg metanu. Z równania wynika, że na spalenie jednej cząsteczki metanu potrzeba dwóch cząsteczek tlenu.
Teraz skup się na obliczeniach masowych. Znając masy atomów węgla (C), wodoru (H) i tlenu (O), możesz obliczyć masę cząsteczki metanu (CH4). Ciepło spalania metanu wynosi: ![]()
Znając masę spalanych substratów (ms), możesz obliczyć energię wydzieloną w wyniku spalania.
Następnie, możesz skorzystać z równania Einsteina, gdzie E to zmiana energii, a c to prędkość światła, aby obliczyć zmianę masy ![]()
Warto pamiętać, że masa powstałych produktów reakcji jest różnicą między masą substratów, a zmianą mas.
W ten sposób oblicz, ile tlenu jest potrzebne do spalenia 1 kg metanu oraz masę powstałych produktów reakcji.