Narysuj wzory elektronowe kwasu mrówkowego i kwasu octowego i wskaż zdania prawdziwe i zdania fałszywe.
Kwas mrówkowy:
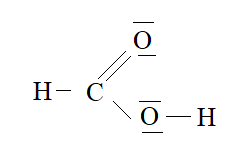
Kwas octowy:
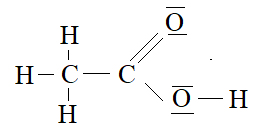
1. W kwasie mrówkowym jest taka sama liczba wiązań typu 𝜋 jak w kwasie octowym. - P
2. Kwas mrówkowy jest kwasem słabszym od kwasu octowego. - F
3. W obu kwasach występuje atom węgla o hybrydyzacji orbitali walencyjnych sp3. - F
4. W roztworach wodnych kwasu mrówkowego i octowego występują wiązania wodorowe. - 4
5. Przy stężeniu 0,1 mol/dm3 stopień dysocjacji kwasu mrówkowego jest większy niż kwasu octowego. - P

Stałe dysocjacji obu kwasów:
HCOOH: 1,8 ∙ 10-4
CH3COOH: 1,8 ∙ 10-5
1. Posiadają jedno wiązanie typu π
2. Słabszym kwasem jest kwas octowy (niższa wartość stałej dysocjacji)
3. W kwasie mrówkowym jedyny atom węgla ma hybrydyzację sp2.
4. Wiązanie wodorowe wystąpi, gdy atom wodoru jest połączony z atomem bardziej elektroujemnego (np. O, F, N) pierwiastka, a cząsteczka musi być relatywnie nieduża.
5. Stopień dysocjacji można wyliczyć z uproszczonego prawa rozcieńczeń:
K = α2∙ c
α = ![]()
Ze wzoru wynika, że czym większa stała dysocjacji K, przy zachowaniu tego samego stężenia, tym większy będzie stopień dysocjacji.

Zadanie 13.
82Zadanie 14.
82Zadanie 16.
82Zadanie 11.
89Zadanie 12.
89Zadanie 19.
93Zadanie 18.
98Zadanie 21.
98Zadanie 21.
103Zadanie 23.
104Zadanie 29.
105Zadanie 10.
109Zadanie 13.
110Zadanie 5.
116Zadanie 6.1
117Zadanie 6.2
117
