Twoim zadaniem jest obliczenie numeru orbity, znając wartość częstotliwości promieniowania emitowanego przez atom wodoru.
![]()
𝑛=?
![]() - energia elektronu na n-tej orbicie, gdzie:
- energia elektronu na n-tej orbicie, gdzie:
![]() – energia elektronu na n-tej orbicie
– energia elektronu na n-tej orbicie
![]() – stała równa energii jonizacji atomu wodoru:
– stała równa energii jonizacji atomu wodoru:
![]()
![]() – numer orbity
– numer orbity
Energia wyemitowanego fotonu podczas przeskoku elektronu z n-tej orbity na czwartą:
![]() , gdzie:
, gdzie:
![]() – energia elektronu na wyższej orbicie
– energia elektronu na wyższej orbicie
![]() – energia wyemitowanego fotonu
– energia wyemitowanego fotonu
![]() – energia elektronu na niższej czwartej orbicie
– energia elektronu na niższej czwartej orbicie
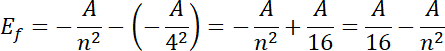
![]() , gdzie:
, gdzie:
![]() – częstotliwość promieniowania
– częstotliwość promieniowania
![]() - stała Plancka (
- stała Plancka (
![]() )
)
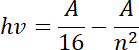
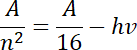
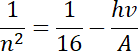
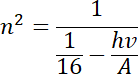
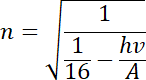
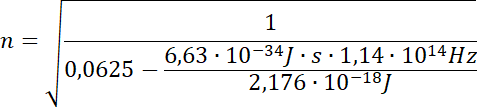
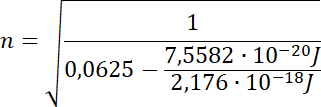
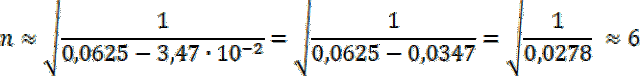
Przeskok elektronu nastąpił z szóstej na czwartą orbitę.

Do rozwiązania zadania konieczna jest znajomość wzoru na energię elektronu na n-tej orbicie:
![]() . Energię fotonu należy wyrazić za pomocą wzoru
. Energię fotonu należy wyrazić za pomocą wzoru
![]() . Energię
. Energię
![]() fotonu możemy również zapisać jako:
fotonu możemy również zapisać jako:
![]() , gdzie w analizowanym przypadku z zadania równanie to zapiszemy w postaci:
, gdzie w analizowanym przypadku z zadania równanie to zapiszemy w postaci:
![]() . Stąd otrzymujemy zapis:
. Stąd otrzymujemy zapis:
![]() , który odpowiednio przekształcony pozwoli na obliczenie szukanej wartości (numeru orbity) :
, który odpowiednio przekształcony pozwoli na obliczenie szukanej wartości (numeru orbity) :
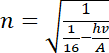 .
.

Zadanie 1.5
28Zadanie 1.17
30Zadanie 1.19
31Pytanie 1.26
32Zadanie 1.28
32Zadanie 3.2
35Zadanie 3.3
35Zadanie 3.4
36Zadanie 3.8
36Zadanie 3.11
37Zadanie 3.12
37Zadanie 3.14
38Zadanie 3.15
39Zadanie 4.2
39Zadanie 4.5
40Zadanie 5.6
41Zadanie 5.7
41Zadanie 5.8
42Pytanie 6.1
43Pytanie 6.4
44Zadanie 6.7
45Zadanie 6.8
45Zadanie 6.10
45Zadanie 6.11
46Zadanie 6.15
47Zadanie 6.16
47Zadanie 6.17
47Zadanie 6.18
47Zadanie 6.19
48Zadanie 6.20
48Zadanie 7.3
48Zadanie 7.5
49Zadanie 7.6
50Zadanie 7.7
50Zadanie 8.2
52Zadanie 8.4
53Zadanie 8.9
53Zadanie 8.10
53Zadanie 8.11
53Zadanie 8.14
54Zadanie 8.16
54Zadanie 8.18
54Zadanie 8.22*
55Zadanie 9.7
58Zadanie 10.6
62Zadanie 10.10
62Zadanie 10.11
62
